[ad_1]
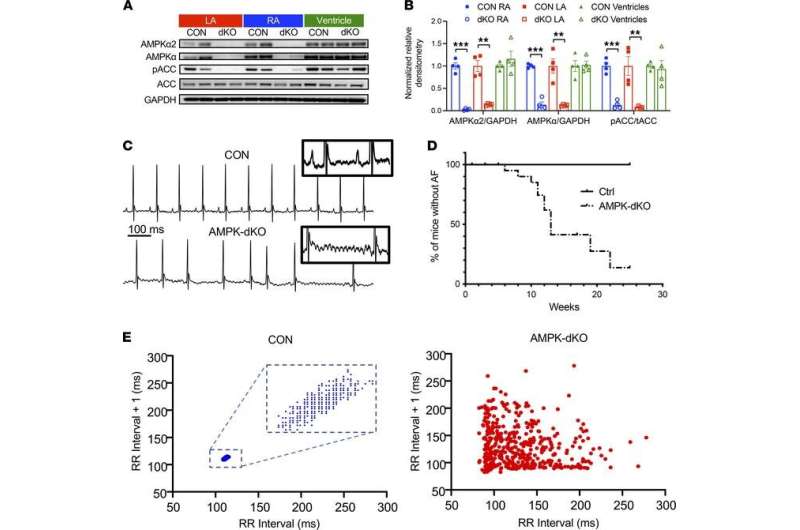
حذف انتخابی دهلیز AMPK منجر به فیبریلاسیون دهلیزی در موش می شود. بیان AMPK و توسعه فیبریلاسیون دهلیزی در AMPK double-KO sarcolipin-Cre Prkaa1fl/fl پرکاا2fl/fl (AMPK-dKO) در مقایسه با کنترل همزاد Prkaa1fl/fl پرکاا2fl/fl موش (CON). (الف) بلاتهای ایمونوبلاتی با آنتیبادیهایی که زیرواحد α2 AMPK، هر دو زیرواحد α1 و α2 AMPK (AMPKα)، هدف پاییندستی AMPK استیل کوآ کربوکسیلاز (ACC) و فرم فسفریله ACC (pACC) در دهلیز چپ (LA) را تشخیص میدهند. دهلیز راست (RA) و بطن چپ. (ب) کمیت سنجی مربوط به باندهای واکنش پذیر. مقادیر میانگین ± SEM n = 6-8 در هر گروه است. ** تست P t. (C) ردیابی ECG در داخل بدن (سرب II) که ریتم سینوسی طبیعی را در CON و فیبریلاسیون دهلیزی در موش AMPK-dKO دهلیزی در 6 هفتگی نشان میدهد. Inset ها نماهای بزرگنمایی شده را نشان می دهند که فعالیت الکتریکی موج P دهلیزی بسیار سازمان یافته را در امواج فیبریلاتور CON و البته در موش های AMPK-dKO نشان می دهد. نوارهای مقیاس: 100 میلیثانیه (D) تجزیه و تحلیل Kaplan-Meier که بقای 6 ماهه بدون رویداد از فیبریلاسیون دهلیزی را در موشهای CON (n = 18) در مقابل موشهای AMPK-dKO (n = 23) نشان میدهد، P JCI Insight (2022). DOI: 10.1172/jci.insight.141213
تحقیقات دانشکده پزشکی ییل نشان می دهد که پروتئین کیناز که تنظیم کننده اصلی متابولیسم سلولی است برای جلوگیری از فیبریلاسیون دهلیزی حیاتی است. این تحقیق در 22 آوریل در مجله منتشر شد JCI Insight.
دکتر لاورنس اچ یانگ، استاد پزشکی و فیزیولوژی سلولی و مولکولی و نویسنده ارشد این مطالعه، گفت که ارتباط بین استرس متابولیک و فیبریلاسیون دهلیزی به خوبی درک نشده است.
یانگ می گوید: «ما باید مکانیسم های مرتبط با بیماری متابولیک و پیدایش فیبریلاسیون دهلیزی را درک کنیم. “هدف ما تعریف نقش AMPK در جلوگیری از بازسازی مولکولی، الکتروفیزیولوژیکی و ساختاری دهلیزی بود.”
تیم تحقیقاتی از موش های تغییر یافته ژنتیکی برای بررسی اثرات بیولوژیکی آنزیم پروتئین کیناز فعال شده با AMP (AMPK) در دهلیزها، اتاق های فوقانی قلب، استفاده کردند. AMPK برای حفظ عملکرد متابولیک در قلب و سایر اندام ها ضروری است. با همکاری Fadi G. Akar، دانشیار که این مطالعه را نویسندگی کرده بود، آزمایشگاه Young تأثیر نامطلوب حذف ژنتیکی AMPK بر بازسازی مولکولی، الکتریکی و ساختاری دهلیزی را نشان داد که به فیبریلاسیون دهلیزی پایدار منجر شد.
نویسندگان همچنین دریافتند که Pitx2c و Mef2c – فاکتورهای رونویسی که در رشد قلبی ضروری هستند – تحت تأثیر حذف AMPK قرار می گیرند و در حفظ برنامه ریزی مولکولی دهلیزی طبیعی بسیار مهم هستند.
در حالی که تحقیقات بیشتری مورد نیاز است، یافتهها نشان میدهند که کاهش فعالیت AMPK که در بیماران مسن مبتلا به بیماریهای متابولیک، مانند دیابت و چاقی رخ میدهد، ممکن است به بزرگ شدن دهلیزی و ایجاد اختلال در عملکرد الکتریکی کمک کند. این کشف می تواند به درمان های بالقوه ای برای فیبریلاسیون دهلیزی منجر شود که علت اصلی بیماری را برطرف می کند.
فیبریلاسیون دهلیزی شایع ترین آریتمی یا اختلال ریتم قلب است. بروز فیبریلاسیون دهلیزی در حال افزایش است و این آریتمی ها باعث لخته شدن خون، سکته مغزی، نارسایی قلبی و سایر عوارض قلبی عروقی می شوند.
فیبریلاسیون دهلیزی به طور قابل توجهی خطر ابتلا به عوارض جدی و مرگ ناشی از COVID-19 را افزایش می دهد.
کوین ان. سو و همکاران، پروتئین کیناز فعال شده با AMP دهلیزی برای جلوگیری از اختلال در تنظیم تحریک پذیری الکتریکی و فیبریلاسیون دهلیزی حیاتی است. JCI Insight (2022). DOI: 10.1172/jci.insight.141213
ارائه شده توسط دانشگاه ییل
نقل قول: نقش سیگنال دهی متابولیک در پیشگیری از فیبریلاسیون دهلیزی (2022، 26 آوریل) بازیابی شده در 26 آوریل 2022 از https://medicalxpress.com/news/2022-04-role-metabolic-atrial-fibrillation.html
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.
[ad_2]