[ad_1]
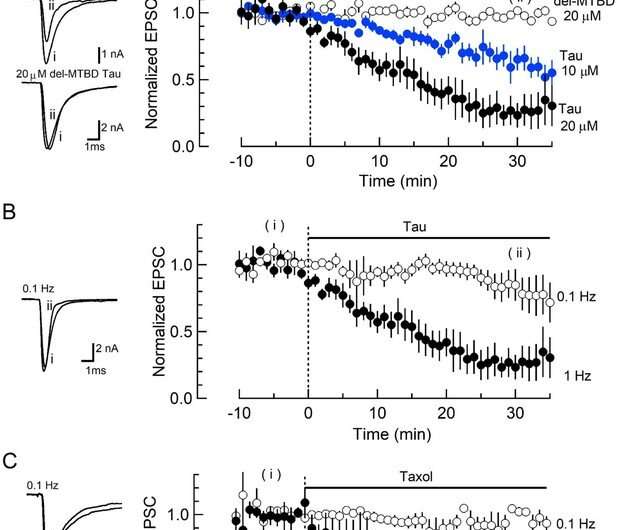
نوع وحشی (WT) h-tau بارگذاری شده در پایانه های پیش سیناپسی، انتقال سیناپسی تحریکی را مهار کرد. اعتبار: تتسویا هوری و همکاران، eLife (2022). DOI: 10.7554/eLife.73542
بیماری آلزایمر یک اختلال مغزی است که باعث مرگ نورون ها می شود و به آرامی حافظه و مهارت های تفکر را از بین می برد. این شایع ترین نوع زوال عقل است که حدود 50 میلیون نفر را در سراسر جهان تحت تاثیر قرار می دهد و یک مسئله جدی برای جامعه فوق العاده سالخورده ژاپن است. علیرغم شیوع آن، علل آن به خوبی شناخته نشده است و گزینه های درمانی محدود است.
اکنون، تیمی از دانشمندان در ژاپن نشان دادهاند که چگونه تاو بیش از حد – یک پروتئین کلیدی که در بیماری آلزایمر نقش دارد – سیگنالهای بین نورونهای مغز موشها را مختل میکند. این مطالعه که اخیراً در eLife، می تواند مسیرهای جدیدی را برای درمان علائم و حتی توقف پیشرفت بیماری آلزایمر و سایر اختلالات عصبی باز کند.
تاو در نورونها تولید میشود، جایی که به مونتاژ میکروتوبولها – رشتههای بلند و نازکی که ساختار سلولی را حفظ میکنند و مسیرهایی را برای حمل و نقل درون سلولی ایجاد میکنند- متصل میشود و باعث تقویت آن میشود. تاو معمولاً در این حالت محدود وجود دارد یا در مایعی که سلول را پر می کند حل می شود.
با این حال، در برخی از اختلالات عصبی، که معروفترین آنها در بیماری آلزایمر است، سطح تاو محلول در نواحی خاصی از مغز بسیار بالا میرود و در ساختارهای نامحلولی به نام درهمتنیدگیهای نوروفیبریلاری تجمع مییابد.
پروفسور تومویوکی تاکاهاشی، نویسنده ارشد این مطالعه گفت: “بسیاری از دانشمندان بر تاثیر این گرههای نوروفیبریلاری قابل مشاهده که نشانه آلزایمر هستند تمرکز میکنند، اما در واقع، این سطوح نامرئی تاو محلول است که بیشترین ارتباط را با زوال شناختی دارد.” و رئیس واحد عملکرد سیناپسی سلولی و مولکولی در OIST.
این تحقیق ده سال پیش آغاز شد، زمانی که تیم او به تأثیر سطوح بالای تاو محلول بر روی انتقال سیگنال در کاسه گل هلد – بزرگترین سیناپس در مغز پستانداران – پرداخت. سیناپس ها مکان هایی هستند که در آن دو نورون با یکدیگر تماس و ارتباط برقرار می کنند. هنگامی که یک سیگنال الکتریکی به انتهای یک نورون پیش سیناپسی می رسد، پیام رسان های شیمیایی که به عنوان انتقال دهنده های عصبی شناخته می شوند، از “بسته های” غشایی به نام وزیکول در شکاف بین نورون ها آزاد می شوند. هنگامی که انتقال دهنده های عصبی به نورون پس سیناپسی می رسند، یک سیگنال الکتریکی جدید ایجاد می کنند.
تیم تحقیقاتی پروفسور تاکاهاشی با استفاده از موش، تاو محلول را به انتهای پیش سیناپسی در کاسه گل هلد تزریق کردند و دریافتند که سیگنال های الکتریکی تولید شده در نورون پس سیناپسی به طور چشمگیری کاهش می یابد.
سپس دانشمندان تاو و میکروتوبولها را با فلورسنت برچسبگذاری کردند و مشاهده کردند که تاو تزریق شده باعث تجمع جدید بسیاری از میکروتوبولها در پایانه پیشسیناپسی میشود.
با این حال، زمانی که آنها پروتئین تاو جهش یافته را به جای آن تزریق کردند که فاقد محل اتصال لازم برای جمع آوری میکروتوبول ها بود، هیچ تاثیری بر انتقال سیناپسی وجود نداشت.
پروفسور تاکاهاشی توضیح داد: “این به ما گفت که کاهش سیگنال سیناپسی به وضوح با این میکروتوبول های تازه مونتاژ شده مرتبط است.”
دومین سرنخ مهم این بود که افزایش تاو تنها انتقال سیگنال های فرکانس بالا را کاهش می دهد، در حالی که انتقال فرکانس پایین بدون تغییر باقی می ماند. سیگنال های فرکانس بالا معمولاً در کنترل شناخت و حرکت نقش دارند.
محققان مشکوک بودند که چنین تأثیر انتخابی بر انتقال فرکانس بالا ممکن است به دلیل مسدود شدن بازیافت وزیکول باشد.
بازیافت وزیکول یک فرآیند حیاتی برای آزادسازی انتقال دهنده های عصبی در سراسر سیناپس است زیرا وزیکول های سیناپسی باید با غشای انتهایی پیش سیناپسی در فرآیندی به نام اگزوسیتوز ترکیب شوند. این وزیکولها سپس با اندوسیتوز اصلاح میشوند و با انتقالدهنده عصبی دوباره پر میشوند تا دوباره مورد استفاده قرار گیرند. اگر هر یک از مراحل بازیافت وزیکول مسدود شود، به سرعت سیگنالهای فرکانس بالا را تضعیف میکند که به اگزوسیتوز بسیاری از وزیکولها نیاز دارد.
دانشمندان دریافتند که سطوح بالای تاو محلول در درجه اول باعث اختلال در اندوسیتوز می شود. فقدان وزیکول های اصلاح شده بازیافت را مختل می کند و در نهایت اگزوسیتوز را به عنوان یک اثر ثانویه کند می کند.
نکته مهم این است که محققان دریافتند دارویی به نام نوکودازول که تجمع میکروتوبولهای جدید را مسدود میکند، مانع از آسیب رساندن تاو تزریقی به اندوسیتوز میشود.
گام بعدی برای محققان این بود که دقیقا بفهمند چگونه میکروتوبولهای اضافی باعث ایجاد بلوک اندوسیتوز میشود.
در حین جستجوی ارتباط بین میکروتوبول ها و اندوسیتوز، تیم متوجه شد که دینامین، پروتئین بزرگی که وزیکول ها را از غشای سطحی در مرحله نهایی اندوسیتوز جدا می کند، در واقع به عنوان پروتئینی که به میکروتوبول ها متصل می شود، کشف شد، اگرچه اطلاعات کمی در مورد آن وجود دارد. سایت الزام آور
هنگامی که دانشمندان با برچسب فلورسنت تاو، میکروتوبول ها و دینامین را نشان دادند، دریافتند که پایانه های پیش سیناپسی که با تاو تزریق شده بودند، افزایش دینامین باند شده را نشان دادند و از ایفای نقش پروتئین در اندوسیتوز جلوگیری می کردند.
در نهایت، این تیم پپتیدهای زیادی را با توالیهای تطبیق آمینو اسیدها با بخشهایی از پروتئین دینامین ایجاد کردند تا ببینند آیا هر یک از آنها میتواند از اتصال دینامین به میکروتوبولها جلوگیری کند و بنابراین نقص سیگنالدهی ناشی از پروتئین تاو را نجات دهد. هنگامی که یکی از این پپتیدها به نام PHDP5 همراه با تاو تزریق شد، اندوسیتوز و انتقال سیناپسی نزدیک به سطح نرمال باقی ماند.
در حرکت رو به جلو، محققان قصد دارند این پپتید را در مدلهای موش آلزایمر که سطح تاو محلول را افزایش میدهند، آزمایش کنند. این موش ها توانایی خود را برای یادگیری و ایجاد خاطرات جدید در حدود 6 تا 8 ماهگی از دست می دهند و تیم امیدوار است که این پپتید بتواند از این اختلال حافظه جلوگیری یا معکوس کند.
پروفسور تاکاهاشی گفت: “برای این منظور، ما باید PHDP5 را به گونه ای اصلاح کنیم که بتواند به سد خونی مغزی نفوذ کند. اگر این پپتید در این مدل های موش کار کند، می تواند به عنوان یک ابزار درمانی موثر برای بیماری آلزایمر عمل کند.”
دانشمندان از نحوه عملکرد بیهوشی عمومی پرده برداری کردند
Tetsuya Hori و همکاران، مونتاژ میکروتوبول توسط تاو باعث اختلال در اندوسیتوز و انتقال عصبی از طریق ترسیب دینامین در مدل سیناپس بیماری آلزایمر می شود. eLife (2022). DOI: 10.7554/eLife.73542
eLife
ارائه شده توسط دانشگاه فارغ التحصیلان موسسه علم و فناوری اوکیناوا
نقل قول: گشودن نقش تاو در بیماری آلزایمر (2022، 22 ژوئن) در 22 ژوئن 2022 از https://medicalxpress.com/news/2022-06-untangling-role-tau-alzheimer-disease.html بازیابی شده است.
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.
[ad_2]