[ad_1]
توسط Kerstin Wagner، Leibniz-Institut für Alternsforschung – Fritz-Lipmann-Institut eV (FLI)
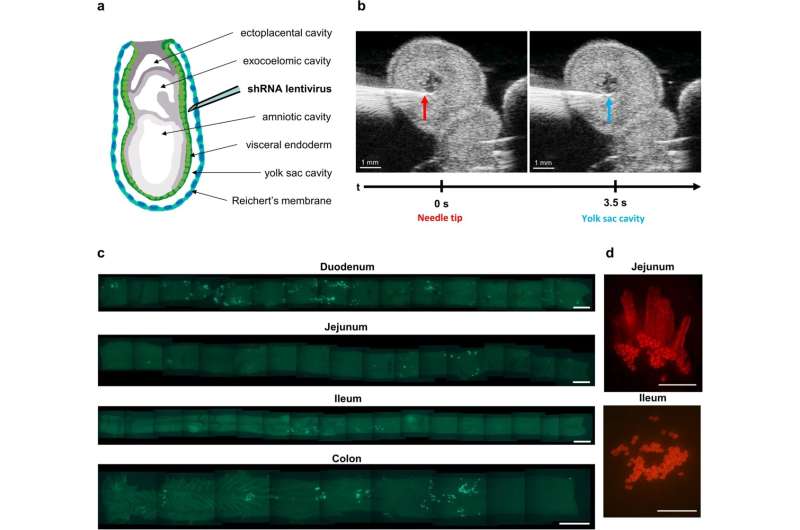
تزریق لنتی ویروسی جنین موش E8.0 به هدف گیری پایدار اپیتلیوم روده در موش های بالغ دست می یابد. اعتبار: زیست شناسی BMC (2023). DOI: 10.1186/s12915-022-01466-1
روده با طول حدود هشت متر و برجستگی های انگشتی شکل بی شمارش که به پرز معروف است، بزرگترین سطح تماس در قسمت داخلی بدن ما را نشان می دهد که با غذای گرفته شده در تماس است.
به عنوان مهم ترین اندام دستگاه گوارش، وظایف اصلی آن شامل جذب مواد مغذی از غذا، تامین انرژی و دفع متابولیت های مضر است. سد روده ای به عنوان نوعی دیواره محافظ عمل می کند که از ورود میکروب ها یا مواد خارجی به بدن جلوگیری می کند و بنابراین تأثیر تعیین کننده ای بر سلامت (دفاع ایمنی) دارد.
بخشی از دیواره روده پوشش روده (اپیتلیوم روده) است که داخل روده را می پوشاند و نقش مهمی در جذب آب، الکترولیت ها و مواد مغذی دارد. همچنین در معرض یک فرآیند تجدید مداوم است و سریعترین بافت خود تجدید شونده در پستانداران بالغ است، با زمان بازسازی 3-10 روز.
علیرغم عملکردهای متنوع روده و اهمیت بسیار زیاد آن برای سلامتی، تا کنون اطلاعات کمی در مورد اینکه کدام ژن در هضم یا در ایجاد بیماری های روده ای نقش دارند – علیرغم تحقیقات فشرده – شناخته شده است.
محققان مؤسسه سالمندی لایبنیتس – موسسه فریتز لیپمن (FLI) در ینا، آلمان، با همکاری شرکای مرکز سرطان فرد هاچینسون در سیاتل، ایالات متحده، اکنون به یک نقطه عطف مهم دست یافتهاند: آنها روش جدیدی را توسعه دادهاند که در از یک سو مطالعات ژنتیکی را برای تمام نواحی روده ممکن میسازد و از سوی دیگر میتوان از آن برای بررسی دقیقتر تأثیر ژنها بر سرطانزایی، فرآیند پیری و تعاملات میکروبیوم میزبان استفاده کرد.
نتایج تحقیقات فعلی اکنون در مجله منتشر شده است زیست شناسی BMC.
تجزیه و تحلیل جهش تک ژنی در مقابل غربالگری تعداد زیادی ژن
K توضیح می دهد: “با استفاده از جهش های ژرمینال خاص، در حال حاضر می توان ژن های فردی را در اپیتلیوم روده خاموش کرد و تاثیر آنها را بررسی کرد. اما علیرغم تلاش های متعدد، هنوز روشی وجود ندارد که بتوان از آن برای مطالعه همزمان تعداد زیادی از ژن ها استفاده کرد.” لنهارد رودولف، رهبر گروه تحقیقاتی در FLI و استاد پزشکی مولکولی در FSU Jena. اما چنین رویکردی ضروری است، زیرا ژنوم انسان دارای بیش از 25000 ژن است که حدود سه چهارم آن در روده ما فعال است.
پروفسور رودولف می افزاید: «علاوه بر این، تحقیق در مورد عملکرد این ژن ها از طریق آنالیزهای هدفمند جهش تک ژنی بسیار پرهزینه و همچنین زمان بر است. در اصل، القای جهش در سلول های منفرد یک بافت با استفاده از ذرات ویروس حاوی توالی های ژنی خاص امکان پذیر است. با این رویکرد می توان مطالعات غربالگری روی تعداد زیادی از ژن ها را به طور همزمان انجام داد.
این محقق سلولهای بنیادی میگوید: امروزه از این روش برای بررسی سلولهای بنیادی پوست، کبد و خون استفاده میشود، اما تاکنون قابل انتقال به اپیتلیوم روده نبوده است، زیرا سلولهای بنیادی اپیتلیوم روده عمیق هستند. در دخمه ها (جیب های عمیق بین پرزها) پنهان شده و بنابراین دسترسی به انتقال ژن از طریق ذرات ویروسی بسیار دشوار است.
معایب روش های تحقیق قبلی
دکتر جورج بی. گارساید از FLI، نویسنده اصلی این مطالعه، میافزاید: «روشهای شناختهشده در حال حاضر برای مطالعه اپیتلیوم روده از ارگانوئیدهای روده، اندامهای کوچک کوچکی که در کشت سلولی رشد میکنند و با افزودن ویروسها اصلاح ژنتیکی میشوند، استفاده میکنند».
این اندامهای کوچک اصلاحشده سپس به اپیتلیوم روده موشهای دارای نقص ایمنی تزریق میشوند و تأثیر ژنها بر عملکرد روده بررسی میشود.»
با این حال، این روش دارای چندین نقطه ضعف است. ارگانوئیدها ابتدا باید در کشت سلولی در آزمایشگاه رشد و تکثیر شوند قبل از اینکه بتوانند توسط ناقل های ویروسی خاص اصلاح ژنتیکی شوند. همه اینها خارج از ارگانیسم اتفاق می افتد، به این معنی که اندام های کوچک فاقد محیط طبیعی خود هستند، که با این حال، رشد طبیعی و نگهداری اپیتلیوم روده را تنظیم می کند.
در اثر شرایط رشد غیرطبیعی در کشت، تغییراتی در سلولهای بنیادی روده رخ میدهد که پس از آن عملکرد ژنها را در شرایط طبیعی منعکس نمیکنند.
مشکلاتی نیز در حین پیوند ایجاد می شود، زیرا به دلیل طول روده و دسترسی ضعیف از خارج، پیوند ارگانوئیدها محدود به کولون تحتانی باقی می ماند و کارایی کلی پایینی دارد و مطالعه را تنها به چند ژن محدود می کند.
به دلیل تمام این محدودیت ها و مشکلات، یافتن روش جدیدی ضروری بود که امکان درج تغییرات ژنتیکی را در محل، مستقیماً در محیط طبیعی اپیتلیوم دست نخورده روده و همچنین امکان مطالعه عملکرد اپیتلیوم روده را فراهم کند. دکتر گارساید می گوید: ژن های متعدد در اپیتلیوم طبیعی روده. این همچنین دارای مزایایی است زیرا سلولها در کشت میتوانند تحت انتخاب غیرطبیعی و تغییراتی قرار گیرند که شناسایی عملکرد ژن در سلولهای اصلاح نشده را مختل میکند.
روش جدید برای مطالعه اپیتلیوم روده
محققان موفق به ایجاد روشی قوی و قابل تکرار شدند که امکان وارد کردن تعداد زیادی از تغییرات ژنتیکی را در سلولهای بنیادی اپیتلیوم طبیعی اصلاح نشده روده بدون نیاز به پیوند فراهم میکند. پروفسور رودولف گزارش می دهد: “ما برای مطالعه خود از موش های آزمایشگاهی استفاده کردیم که از بسیاری جهات شرایط فیزیولوژیکی اپیتلیوم روده انسان را منعکس می کنند.”
با توجه به دسترسی دشوار به محل تشریحی سلولهای بنیادی، که عمیقاً در دخمههای اپیتلیوم روده موشهای بالغ پنهان شدهاند، در طول رشد جنینی اولیه موشها از تکنیک میکرواینجکشن ویژه استفاده شد. این به این دلیل است که در این مرحله اولیه از رشد، روده هنوز به سمت بیرون چرخیده است و آن را برای معرفی تغییرات ژنتیکی هدفمند در دسترس تر می کند.
پتانسیل بسیار زیاد – طیف وسیعی از کاربردها
یافتههای این مطالعه نشان میدهد که تکنیک جدید میتواند برای مطالعه عملکرد ژن در اپیتلیوم روده هم در حین رشد و هم در حیوانات بالغ مورد استفاده قرار گیرد. علاوه بر این، این روش پتانسیل شناسایی ژنهایی را دارد که بر سرطانزایی، پیری و برهمکنشهای بین میکروبیوم (باکتریهای روده) و میزبان تأثیر میگذارند.
مزیت اصلی این روش این است که اجازه می دهد تا غربالگری های ژنتیکی in vivo در اپیتلیوم روده دست نخورده موش و احتمالاً در سایر اندام های مدل انجام شود. بنابراین، تمام نواحی دستگاه گوارش از جمله معده، روده کوچک و کولون را می توان از نظر ژنتیکی اصلاح و مطالعه کرد.
نکته قابل توجه این است که این روش را می توان در سایر اندام های مشتق شده از اندودرم مانند پانکراس، کبد، مثانه و ریه نیز به کار برد، به طوری که این روش می تواند در سایر زمینه های تحقیقاتی نیز بسیار مفید باشد. توسعه این روش برای مطالعه این اندام ها از اهمیت بالایی برخوردار است و می تواند به ویژه کشفیات مربوط به زیست شناسی، عملکرد و توسعه بیماری های اپیتلیوم روده را تسریع بخشد.
اطلاعات بیشتر:
جورج بی. گارساید و همکاران، هدف قرار دادن سلول های بنیادی درجا لنتی ویروسی در اپیتلیوم روده ای بدون اختلال، زیست شناسی BMC (2023). DOI: 10.1186/s12915-022-01466-1
ارائه شده توسط Leibniz-Institut für Alternsforschung – Fritz-Lipmann-Institut eV (FLI)
نقل قول: روش جدید مطالعات ژنتیکی عملکرد و بیماریهای اپیتلیوم روده را تسهیل میکند (2023، 23 ژانویه) در 23 ژانویه 2023 از https://medicalxpress.com/news/2023-01-method-genetic-function-diseases-intestinal بازیابی شده است. html
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.
[ad_2]