[ad_1]
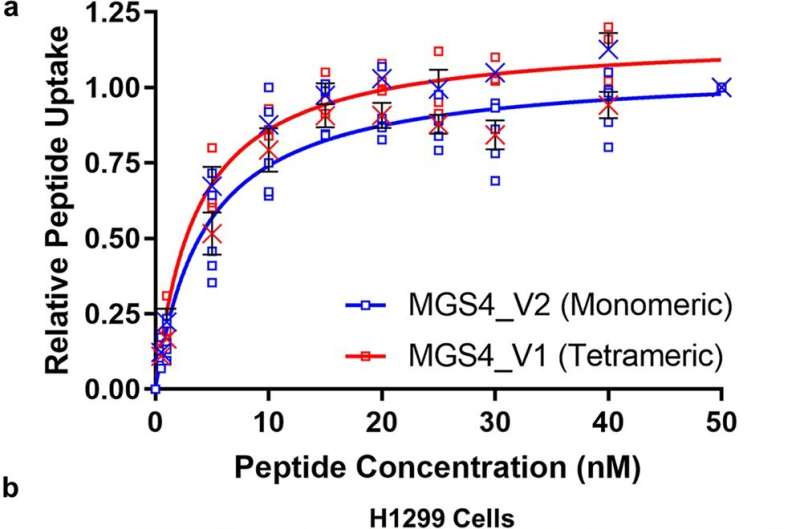
مونومر و تترامر MGS4 اتصال، درونی سازی و مکان درون سلولی مشابهی دارند. الف، اتصال و درونی سازی MGS4_V1 تترامر و MGS4_V2 مونومر روی سلول های زنده H1299 در کشت. سلول ها با پپتید کونژوگه به استرپتاویدین-فیکواریترین به مدت 1 ساعت در دمای 37 درجه سانتی گراد انکوبه شدند. پپتید غیر درونی حذف شد و سلول ها با فلوسایتومتری آنالیز شدند. b، سلول های H1299 با MGS4_V1 یا MGS4_V2 کونژوگه به استرپتاویدین-الکسا فلور 555 (قرمز) به مدت 1 ساعت انکوبه شدند، شسته شدند، تثبیت شدند و با WGA-Alexa Fluor 488 (سبز، غشای سلولی) و هسته آنالیز شدند. توسط میکروسکوپ فلورسانس نوار مقیاس نشان دهنده 20 میکرومتر است. MGS4_V1 و MGS4_V2 به درجه ای مشابه درونی می شوند و در یک مقصد مشابه بومی سازی می شوند. پپتیدهای مونومر MGS4 کوتاه شده دارای EC50 مشابه به عنوان پپتید تمام قد والدین هستند. اندازه گیری های فردی نشان داده شده است. میانگین به صورت “X” نشان داده می شود و نوارهای خطای سیاه نشان دهنده خطای استاندارد برای حداقل سه تکرار آزمایشی (SEM) است. تمام داده های اتصال اصلی و تحلیل رگرسیون غیر خطی داده ها در مواد تکمیلی گنجانده شده است. اعتبار: زیست شناسی ارتباطات (2023). DOI: 10.1038/s42003-022-04385-7
سرطان ریه سالانه بیش از هر نوع سرطان دیگری در سراسر جهان جان خود را از دست می دهد. بر اساس گزارش سازمان بهداشت جهانی، تخمین زده میشود که در سال 2020 حدود 1.8 میلیون نفر بر اثر سرطان ریه جان خود را از دست دادند. درمانهای کنونی بر یکی از دو روش متکی هستند: شیمیدرمانی عمومی که عوارض جانبی شدیدی را بر بیماران سرطانی ایجاد میکند، یا هدف قرار دادن تومورهایی با جهشهای بسیار خاص که ممکن است چنین نباشد. برای بسیاری از بیماران اعمال می شود که هر دوی آنها مبارزه با بیماری را چالش برانگیز می کند.
محققان SRI International یک پپتید جدید – مولکولی که حاوی دو یا چند اسید آمینه است – طراحی و بهینهسازی کردهاند تا بهعنوان وسیلهای برای انتقال داروها برای درمان سرطان ریه سلولهای غیرکوچک، که اکثر موارد سرطان ریه را تشکیل میدهد، عمل کند. این پپتید، در مطالعه اخیر منتشر شده در زیست شناسی ارتباطات طبیعت، می تواند داروهای ضد سرطان بزرگی را حمل کند و با موفقیت سلول های سرطانی را هدف قرار دهد، به آنها متصل شود و فرآیندی را برای کشیدن پپتید و محموله آن به داخل آغاز کند.
کاتلین براون، معاون سیستمهای دارورسانی در بخش علوم زیستی SRI و نویسنده اصلی مقاله، گفت: با پپتیدهای خود، میتوانیم محمولههای بزرگی را در داخل سلولی تحویل دهیم که در غیر این صورت نمیتوانست از غشای سلولی عبور کند. این روش اساساً دری را برای کشیدن داروها به درون عملکرد سلول های تومور باز می کند و در عین حال از سلول های سالم اجتناب می کند و عوارض جانبی بالقوه را به حداقل می رساند.
در حال حاضر، بیشتر داروهای سرطانی که به طور مشابه مورد هدف قرار میگیرند، توسط آنتیبادیهایی عرضه میشوند که به گیرندههای خاصی روی سطح سلول سرطانی متصل میشوند. اما استفاده از پپتیدها به جای آنتی بادی چندین مزیت دارد. اولاً، پپتیدها مولکولهای بسیار کوچکتری هستند، به این معنی که میتوانند به عمق تومور نفوذ کنند. دوم، پپتیدها را می توان به صورت شیمیایی کنار هم قرار داد، در حالی که آنتی بادی ها باید به صورت بیولوژیکی در سلول ها تولید شوند. فرآیند شیمیایی سریعتر، کم هزینه تر است و به محققان کنترل دقیق تری بر نتیجه نهایی می دهد.
براون گفت: «از آنجایی که ما آنها را به صورت شیمیایی میسازیم، انعطافپذیری زیادی در نحوه ترکیب دارو داریم. ما میتوانیم هر دارو یا محمولهای را که میخواهیم بگذاریم، دقیقاً میدانیم کجاست و میتوانیم آن را با ابزارهایی که در آزمایشگاه داریم اصلاح کنیم.»
براون و همکارانش برای یافتن یک پپتید با مجموعه ای از صفات مناسب، از یک فرآیند انتخاب اختصاصی برای غربال کردن کتابخانه ای از میلیاردها گزینه بالقوه استفاده می کنند. در این مورد، آنها به یک پپتید نیاز داشتند که بتواند با موفقیت سلول های سرطانی را جستجو کرده و به آنها متصل شود و در عین حال سلول های سالم را به حال خود رها کند. می تواند فرآیندهای بیولوژیکی را برای کشیدن سریع پپتید و محموله آن به داخل سلول ایجاد کند. و در حین گردش در بدن تخریب نمی شود.
براون گفت: “ما برای شروع یک نشانگر سطح سلولی خاص را هدف قرار نمی دهیم.” ما کاری را انجام میدهیم که به عنوان یک انتخاب بیطرفانه شناخته میشود، که اساساً به این معنی است که به سلولها اجازه میدهیم بهترین پاسخ را به ما بگویند.
هنگامی که براون و تیمش پپتیدی با ویژگیهای مناسب را شناسایی کردند که به عنوان MGS4 شناخته میشود، آن را بهینهسازی کردند تا تا حد امکان مؤثر باشد و آن را با پروتئین سمی به نام ساپورین آزمایش کردند که به خودی خود نمیتواند به طور مؤثر وارد سلولها شود. آنها دریافتند که MGS4 با موفقیت ساپورین را به تومورهای سرطان ریه در موش ها رساند و پس از 18 روز درمان، تومورهای موش هایی که ساپورین متصل به MGS4 دریافت کردند، نصف اندازه تومور در موش های درمان نشده یا در موش هایی بود که به خودی خود ساپورین دریافت کردند.
کار آنها نشان می دهد که MGS4 می تواند یک ابزار ارزشمند در توسعه درمان های هدفمند برای سرطان ریه باشد. و از آنجا که می تواند انواع داروها را حمل کند، محققان تازه شروع به کشف پتانسیل آن برای تسهیل درمان کرده اند.
براون گفت: “این سم پروتئینی اولین مفهوم درمانی ما است، اما آنچه واقعا مهم است این است که این پپتید قادر است درمان های بزرگ، سمی و بیولوژیکی را در داخل سلول تومور ارائه دهد.” ما واقعا امیدواریم که بتوانیم این پپتید را گرفته و در چندین کاربرد مختلف با چندین روش درمانی مختلف استفاده کنیم.”
اطلاعات بیشتر:
Curtis A. Allred و همکاران، تحویل داخل سلولی تومور خاص: انتقال پپتید هدایتشده یک سم کاتالیزوری، زیست شناسی ارتباطات (2023). DOI: 10.1038/s42003-022-04385-7
ارائه شده توسط SRI International
نقل قول: دانشمندان پپتیدی تولید کردند که تومورهای ریه را هدف قرار میدهد و مواد درمانی را در داخل سلولها ارائه میکند (2023، 1 فوریه) که در 1 فوریه 2023 از https://medicalxpress.com/news/2023-02-scientists-peptide-lung-tumors-therapeutics.html بازیابی شده است.
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.
[ad_2]