[ad_1]
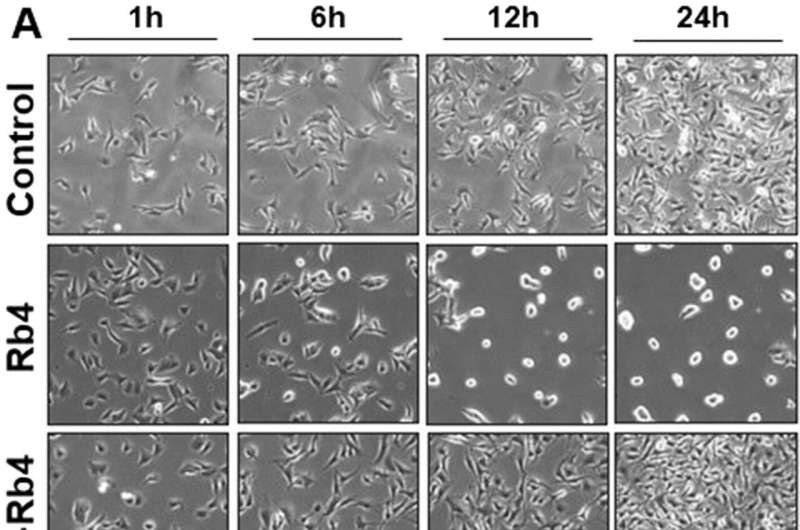
تصاویر فاز تایم لپس سلول های ملانوما B16F10-Nex2 تحت درمان با Rb4 و Scr-Rb4. (الف) پانل ها میدان های نماینده سلول های B16F10-Nex2 پس از کنترل، تیمار Rb4 یا Scr-Rb4 برای 1، 6، 12 و 24 ساعت انکوباسیون هستند. از دست دادن مورفولوژی و عدم تکرار برای سلول های تیمار شده با Rb4 مشاهده شد. (B) پانلهای نماینده سلولهای B16F10-Nex2 تیمار شده با Rb4 به مدت 36، 48 و 72 ساعت که سلولهای مقاوم را نشان میدهند، با رنگ قرمز برجسته شدهاند، مورفولوژی خود را از دست میدهند و پس از قرار گرفتن در معرض طولانی مدت با پپتید Rb4 خوشهبندی شدهاند. نوار، 200 میکرومتر اعتبار: گزارش های علمی (2022). DOI: 10.1038/s41598-022-06429-8
مقاله منتشر شده در گزارش های علمی مطالعهای را توصیف میکند که اثربخشی یک پپتید توسعهیافته توسط دانشمندان برزیلی به نام Rb4 را در مبارزه با پیشرفت سرطان در مدل حیوانی، بهویژه ملانوم بدخیم، نشان میدهد. این مولکول نویدبخش درمان تومورهای مقاوم به دارو است.
کارآزماییهای بالینی in vitro و in vivo نشان داد که Rb4 باعث نکروز در سلولهای ملانوم موش میشود و از زنده ماندن سلولهای سرطانی انسانی جلوگیری میکند. سلول های تومور در این مطالعه یکپارچگی غشای پلاسمایی خود را از دست دادند و میتوکندری ها (ارگانل های تولید کننده انرژی) حتی در غیاب تراکم کروماتین، که یک نشانه مورفولوژیکی آپوپتوز است، گشاد شدند. محققان اذعان می کنند که چگونه این نکروز ایجاد می شود هنوز به درستی درک نشده است.
در موش ها، پپتید متاستاز ریه را کاهش داد و رشد ملانوم زیر جلدی را کند کرد. نتایج نشان میدهد که Rb4 مستقیماً روی تومورها عمل میکند و باعث بیان دو الگوی مولکولی مرتبط با آسیب (DAMPs) میشود که باعث مرگ سلولی ملانومای ایمنی میشود.
ما علوم پایه را در جستجوی مولکول های جدید انجام می دهیم. در این مطالعه Rb4 که از پروتئین پروتئولیپید 2 مشتق شده است. [PLP2]، تمایل به ایجاد نکروز، نوع خاصی از مرگ سلولی، به ویژه در ملانوم را نشان داد، اما چگونگی ایجاد و توسعه این نکروز مشخص نیست. فابریسیو کاسترو ماچادو، یکی از نویسندگان مقاله، به Agência FAPESP گفت: این مقاله برخی از جنبه های ترکیب مورفولوژیکی پپتید و اثرات نهایی تماس با آن را مورد بحث قرار می دهد.
با حمایت FAPESP، گروهی به رهبری لوئیز رودولفو تراواسوس، استاد بازنشسته در UNIFESP، شروع به انجام این تحقیق کردند. نویسندگان مقاله به تراواسوس ادای احترام می کنند که در سال 2020 درگذشت. او بیش از 230 مقاله در مجلات علمی برجسته منتشر کرد که بسیاری از آنها در مورد مطالعات پپتیدها و پپتیدازها (آنزیم هایی که پروتئین ها را به پپتیدها و در نهایت به اسیدهای آمینه منفرد تجزیه می کنند) منتشر کرد. در بیماری های عفونی و سرطان
پروفسور تراواسوس چندین توالی از پپتیدهای فعال زیستی، مولکولهای کوچک بر اساس آنتیبادیهای توسعهیافته توسط ReceptaBio را شناسایی کرد. Rb4 نیز در طول این فرآیند جستجو برای مولکولهای جدید شناسایی شد، اگرچه از آنتیبادیها مشتق نشده است. ما دیگری به نام Rb9 داریم که در آلیس سانتانا مورایس، تحلیلگر تحقیق و توسعه در ReceptaBio و نویسنده مسئول مقاله، گفت: یک مرحله تحقیقاتی پیشرفته تر، با چندین انتشارات و پتنت، اما هنوز در مرحله پیش بالینی است.
در سال 2016، دانشمندان ساختار Rb9 و مکانیسم عمل آن را به عنوان یک مهارکننده سلول های ملانوما توصیف کردند. یک مقاله جدیدتر منتشر شده در سال 2020 نشان داد که Rb9 به عنوان یک تعدیل کننده ایمنی عمل می کند و می تواند برای کنترل پیشرفت تومور استفاده شود.
“چه در دانشگاه و چه در شرکت هایی مانند ReceptaBio، ما باید تلاش ها را برای انجام تحقیقات ترکیب کنیم. ما به دنبال شرکای هستیم تا روند توسعه دارو را تقویت کنیم، که طولانی و پر دردسر است و نیاز به بحث، جزئیات و تبادل تجربیات دارد. مورایس گفت.
نتایج امیدوار کننده
درمانهای جدید سرطان که در سالهای اخیر توسعه یافتهاند شامل شیمیدرمانی مبتنی بر پپتید است. پپتیدها نه تنها به این دلیل که می توانند به غشای سلول های تومور متصل شوند، بلکه به این دلیل که وزن مولکولی کم، نفوذ بافت سلولی خوب و سمیت کم برای بافت طبیعی دارند، مورد توجه روزافزونی قرار گرفته اند. آنها را می توان به عنوان معرف سلولی، لیگاند، واکسن و حامل داروهای سیتوتوکسیک در درمان پپتید به تنهایی یا مواد کونژوگه با پپتید استفاده کرد.
در مطالعه روی عملکرد ضد تومور Rb4، این گروه دریافتند که این پپتید با مورفولوژی، تکثیر و ارتباط سلولهای ملانوم B16F10-Nex2 که در آزمایشگاه کشت شدهاند تداخل دارد. برخلاف گروه شاهد، سلولهای تیمار شده با Rb4 تکثیر نشدند و خوشههایی تشکیل دادند و مورفولوژی طبیعی خود را پس از انکوباسیون حداکثر به مدت 24 ساعت از دست دادند.
علاوه بر این، Rb4 تعداد گرههای متاستاتیک ریه را در مدل ملانوم سیژنیک (شامل بافتهای تومور از موشهایی با ساختار ژنتیکی یکسان) کاهش داد. این نتیجه پس از تزریق داخل وریدی سلول های ملانوما به موش ها مشخص شد. به آنها پنج تزریق داخل صفاقی پپتید (300 میکروگرم به ازای هر حیوان) در روزهای متناوب داده شد که رشد تومور را تا 40 روز به تاخیر انداخت.
میزان بقای موشهای تحت درمان با Rb4 بهطور قابلتوجهی بیشتر از گروه شاهد بود و بقای گروه را تا بیش از 25 درصد و تا 10 روز افزایش داد.
آیا آزمایش خون می تواند به تشخیص سرطان پوست کمک کند؟
Vera SC Maia و همکاران، پپتید Rb4 مشتق از PLP2 باعث مرگ نکروز با واسطه PARP-1 در سلول های ملانوما موش می شود. گزارش های علمی (2022). DOI: 10.1038/s41598-022-06429-8
ناتالیا گیرولا و همکاران، پپتید Rb9 حاوی ناحیه 3 تعیین کننده مکملیت Ig VH، مهاجرت و تهاجم سلول های ملانوما را با برهمکنش با Hsp90 و گیرنده چسبنده با پروتئین G مهار می کند. پپتیدها (2016). DOI: 10.1016/j.peptides.2016.08.006
Fabrício C. Machado و همکاران، اثرات محافظتی تعدیلکننده ایمنی از پپتید چرخهای Rb9 در محیط ملانوم متاستاتیک و درگیری سلولهای دندریتیک، مرزها در ایمونولوژی (2020). DOI: 10.3389/fimmu.2019.03122
نقل قول: پپتید رشد ملانوم را در آزمایشات حیوانی به تاخیر می اندازد (2022، 20 مه) در 20 مه 2022 از https://medicalxpress.com/news/2022-05-peptide-melanoma-growth-animal-trials.html بازیابی شده است.
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.
[ad_2]