[ad_1]
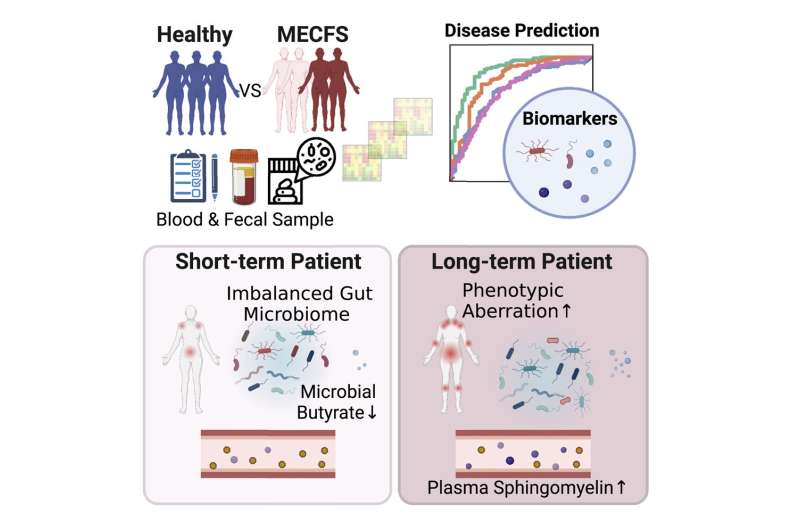
چکیده گرافیکی اعتبار: میزبان سلولی و میکروب (2023). DOI: 10.1016/j.chom.2023.01.001
طی سه سال گذشته، ظهور اثرات بلندمدت مرتبط با COVID-19 منجر به افزایش تمرکز بر بیماری با علائم و نشانههای مشابه – آنسفالومیلیت میالژیک / سندرم خستگی مزمن (ME/CFS) شده است. دو مطالعه منتشر شده در 8 فوریه در مجله میزبان سلولی و میکروب در حال بررسی دقیق ME/CFS هستند زیرا به میکروبیوم و متابولیت هایی که گونه های میکروبی تولید می کنند مربوط می شود.
هر دو مطالعه نشان دادند که ME/CFS با کاهش سطوح میکروبیوم گوارشی میکروبهایی که اسید چرب بوتیرات تولید میکنند مرتبط است. این اختلالات میکروبیوم می تواند تا حدودی توضیح دهد که چگونه سیستم ایمنی در افراد مبتلا به ME/CFS مختل می شود.
جولیا اوه، دانشیار آزمایشگاه جکسون و نویسنده ارشد یکی از این دو مقاله، میگوید: «توجه به این نکته مهم است که این تحقیق ارتباط بین این تغییرات میکروبیوم و ME/CFS را نشان میدهد، نه علت. اما این یافتهها مقدمه بسیاری از آزمایشهای مکانیکی دیگر است که امیدواریم برای درک بیشتر در مورد ME/CFS و علل اساسی آن انجام دهیم.
برنت ال. ویلیامز، استادیار دانشگاه کلمبیا و نویسنده ارشد مقاله دیگر میگوید: «این تحقیق نشان میدهد که نشانههای باکتریایی قوی از دیسبیوز روده در افراد مبتلا به ME/CFS وجود دارد». این امر با شناسایی دقیق اختلالات ساختاری و عملکردی در میکروبیوم در یک بیماری مزمن که بر کیفیت زندگی میلیونها نفر تأثیر میگذارد، به گسترش این زمینه تحقیقاتی در حال رشد کمک میکند.»
ME/CFS یک بیماری مزمن، پیچیده و سیستمیک است که با اختلالات عصبی، ایمنی، اتونوم و متابولیسم انرژی همراه است. دهه هاست که شناخته شده است، اما علل آن هنوز به خوبی شناخته نشده است. مانند کووید طولانی مدت، اعتقاد بر این است که در بیشتر موارد با قرار گرفتن در معرض ویروس ها یا سایر عوامل عفونی ایجاد می شود.
یکی از مواردی که مطالعه ME/CFS را دشوار کرده است این است که تمایل به ناهمگن بودن دارد – همه افراد مبتلا به این بیماری سابقه پزشکی یا علائم مشابهی ندارند. هر دو تیم تحقیقاتی می گویند به همین دلیل انجام مطالعاتی مانند این که داده های تعداد زیادی از بیماران را تجزیه و تحلیل می کند، مهم است. میکروبیوم اخیراً به عنوان یک مشارکت کننده بالقوه و نشانگر زیستی برای ME/CFS ظاهر شده است و مطالعه آن را مهم می کند.
مطالعه Oh از متاژنومیکس شاتگان برای مقایسه نمونههای میکروبیوم از افراد مبتلا به ME/CFS کوتاهمدت (تعریف شده به عنوان مواردی که در چهار سال گذشته تشخیص داده شد؛ ۷۴ بیمار) و ME/CFS طولانیمدت (تعریف شده به عنوان افرادی که علائم بیشتری داشتند، استفاده کرد. بیش از 10 سال؛ 75 بیمار) و همچنین 79 فرد سالم همسان با سن و جنس. محققان همچنین نمونههای پلاسمای شرکتکنندگان را بررسی کردند. این بیماران در مرکز Bateman Horne در سالت لیک سیتی، یوتا، که همکاری دیرینه ای با اعضای آزمایشگاه جکسون دارد، تحت درمان بودند.
تجزیه و تحلیل نشان داد که بیماران مبتلا به بیماری کوتاه مدت تعدادی تغییرات در میکروبیوم های خود با توجه به تنوع داشتند. مهمتر از همه، آنها کاهش میکروبهایی داشتند که بهعنوان تولیدکننده بوتیرات شناخته میشوند. بوتیرات برای محافظت از یکپارچگی سد روده مهم است و همچنین نقش مهمی در تعدیل سیستم ایمنی دارد.
در مقابل، آنهایی که بیماری طولانی مدت داشتند، میکروبیوم های روده داشتند که بازسازی شده بود و بیشتر شبیه به افراد سالم بود. با این حال، این شرکت کنندگان تعدادی از تغییرات در متابولیت ها در پلاسمای خون خود انباشته بودند، از جمله بسیاری از تغییرات مربوط به سیستم ایمنی. آنها همچنین تفاوت هایی در سطح انواع خاصی از سلول های ایمنی در مقایسه با افراد سالم داشتند.
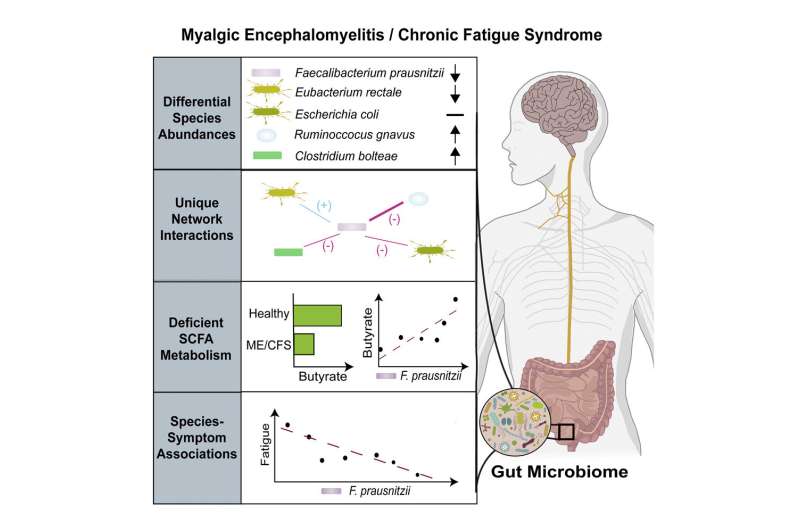
چکیده گرافیکی اعتبار: میزبان سلولی و میکروب (2023). DOI: 10.1016/j.chom.2023.01.004
مطالعه ویلیامز از توالی متاژنومیک تفنگ ساچمه ای برای بررسی میکروبیوم های 106 فرد مبتلا به ME/CFS و 91 فرد سالم که از نظر سن، جنس، جغرافیا و وضعیت اجتماعی-اقتصادی همسان بودند، استفاده کرد. این مطالعه توسط یک گروه تحقیقاتی بینرشتهای و چند نهادی، مرکز راهحلها برای ME/CFS، انجام شد و بیماران را از پنج سایت مختلف در سراسر ایالات متحده بهکار گرفت، که به کنترل تفاوتهای میکروبیومی که ممکن است در مناطق جغرافیایی مختلف وجود داشته باشد کمک کرد. .
این مطالعه همچنین سطوح گونههای میکروبی در مدفوع را مورد بررسی قرار داد. آنالیز پلاسما را شامل نمیشود، اگرچه این گروه قبلاً آنالیزهای متابولومیک پلاسما را از گروه خود در جای دیگری منتشر کرده است. متابولیتهای موجود در مدفوع را مورد بررسی قرار داد که نشاندهنده کاهش سطح متابولیتهای بوتیرات در ME/CFS بود.
مطالعه تیم کلمبیا نشان داد که بین شدت علائم خستگی و سطوح گونههای خاصی از باکتریهای روده، به ویژه باکتری تولیدکننده بوتیرات Faecalibacterium prausnitzii، رابطه قابل توجهی وجود دارد. همچنین بار کلی بیشتر باکتری در مدفوع و اختلال در تعامل بین گونه های باکتریایی در بیماران مبتلا به ME/CFS را نشان داد.
قبل از اینکه این یافتهها مستقیماً در درمانهای جدید اعمال شوند، به تحقیقات بیشتری نیاز است، اما محققان میگویند این یافتهها به توسعه ابزارهای تشخیصی جدید کمک میکند و میتواند به توسعه مدلهای حیوانی بهتر کمک کند.
ویلیامز میگوید: «در حالی که این یافتهها بهطور واضح روابط علّی بین اختلالات در میکروبیوم و علائم را نشان نمیدهند، این روابط میکروبیوم-علائم، اهداف بالقوه قابل عمل و قابل دستکاری را برای آزمایشهای درمانی آینده ارائه میکنند.» این کارآزماییها احتمالاً میتوانند بر روی مداخلات غذایی، پروبیوتیک، پریبیوتیک یا سینبیوتیک متمرکز شوند و میتوانند شواهد مستقیمی را ارائه دهند که نشان میدهد باکتریهای روده بر بروز علائم مزمن تأثیر میگذارند.»
او خاطرنشان می کند که مطالعات آینده او به تقسیم بیشتر بیماران بر اساس ویژگی های بیماریشان کمک خواهد کرد، از جمله آنهایی که دارای شرایطی هستند که اغلب با ME/CFS مرتبط هستند – مانند سندرم روده تحریک پذیر و اختلالات التهابی عصبی. او میگوید: «این به ما کمک میکند تا عوامل میکروبی و متابولومیک خاص مرتبط با این بیماری را مشخص کنیم.
ویلیامز قصد دارد یافته های خود را در مدل های حیوانی بیشتر بررسی کند. او میگوید: «یک مدل موش قابل حمل برای مطالعه اختلالات میکروبیوم روده که در ME/CFS یافت میشود، ابزار مهمی برای ارزیابی فرضیهها، مکانیسمها و درمانهای علّی است.»
اطلاعات بیشتر:
جولیا اوه، چند ویژگی تعامل میکروبیوم روده-میزبان در بیماران کوتاه مدت و بلندمدت آنسفالومیلیت میالژیک/سندرم خستگی مزمن (ME/CFS)، میزبان سلولی و میکروب (2023). DOI: 10.1016/j.chom.2023.01.001
Brent L. Williams، کمبود ظرفیت تولید بوتیرات در میکروبیوم روده با اختلالات شبکه باکتریایی و علائم خستگی در ME/CFS مرتبط است. میزبان سلولی و میکروب (2023). DOI: 10.1016/j.chom.2023.01.004
نقل قول: سندرم خستگی مزمن با تغییرات مشخص در میکروبیوم مرتبط است (2023، 8 فوریه) بازیابی شده در 8 فوریه 2023 از https://medicalxpress.com/news/2023-02-chronic-fatigue-syndrome-distinct-microbiome.html
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.
[ad_2]