[ad_1]
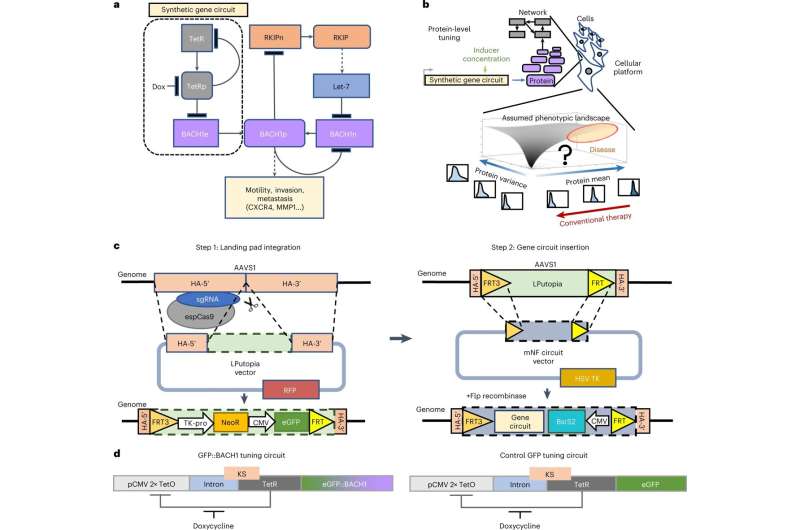
استراتژی دو مرحلهای برای یکپارچهسازی مدار ژن خاص مکان تکرارپذیر آ، نمودار شبکه ای از تعاملات نظارتی و اثرات فنوتیپی برای BACH1 بومی و نابجا. ‘BACH1e’ نشان دهنده ژن BACH1 نابجا است که از طریق مدار ژن mNF معرفی و کنترل می شود، در حالی که ‘BACH1n’ نشان دهنده ژن بومی BACH1 است. ‘BACH1p’ پروتئین BACH1 را نشان می دهد. همین نماد در مورد RKIP نیز صدق می کند. بیک فنوتیپ به عنوان تابعی از میانگین و/یا تغییرپذیری یک یا چند سطح پروتئین یک چشم انداز فنوتیپی را تعریف می کند. درمان مرسوم مناظر فنوتیپی یکنواخت را فرض می کند. با این حال، کشف منظره واقعی نیاز به تنظیم سطح پروتئین دارد. ج، نمودار شماتیک استراتژی دو مرحله ای برای یکپارچه سازی مکان خاص AAVS1 قابل تکرار بارهای ژنتیکی، مانند مدارهای ژن مصنوعی. سمت چپ: درج LP در AAVS1 با CRISPR–Cas9. سمت راست: ادغام LP خاص مبتنی بر RMCE از مدار ژن mNF که بیان همجوشی دو عملکردی eGFP::BACH1 را کنترل می کند. مرحله 2 با استفاده از نشانگرهای مختلف قابل تکرار است. espCas9، افزایش ویژگی SpCas9. NeoR، ژن مقاومت به نئومایسین. دمدار ژن mNF مصنوعی برای تنظیم کنترل شده با dox از TetR که با سطوح پروتئین گزارشگر GFP (mNF-GFP) یا سطوح پروتئین فیوژن GFP::BACH1 (mNF-BACH1) پس از ادغام سایت خاص بیان می شود. KS، دنباله کوزاک. TetO، اپراتور تتراسایکلین. اعتبار: زیست شناسی شیمیایی طبیعت (2023). DOI: 10.1038/s41589-023-01344-z
روش جدیدی که محققان را قادر میسازد تا مقدار یک مهارکننده پروتئین متاستاتیک خاص (BACH1) را در یک سلول جمعآوری یا کاهش دهند، میتواند مسیر جدیدی را در تحقیقات سرطان ایجاد کند که اثربخشی مهارکنندههای پروتئین را برای درمان بیماریها ارزیابی مجدد میکند. این تحقیق که توسط تیمی از دانشمندان دانشگاه استونی بروک هدایت میشود، شامل تنظیم سطوح BACH1 با استفاده از یک مدار ژنی است که در سلولهای متاستاتیک سینه انسان قرار میگیرد. یافته های آنها در منتشر شده است زیست شناسی شیمیایی طبیعت.
زیستپزشکی بر استفاده از مهارکنندههای پروتئین بر این فرض تکیه میکند که کاهش سطح یا فعالیت پروتئین محرک بیماری عموماً هنگام درمان سرطان مفید است. اما به گفته Gábor Balázsi، Ph.D.، نویسنده اصلی “چشم انداز تهاجم غیر یکنواخت با کنترل نویز آگاهانه سطوح فعال کننده متاستاز”، وقتی صحبت از انکوژن ها می شود که پروتئین های محرک سرطان را تولید می کنند و آنها را از طریق “حذف” دستکاری می کنند. رویکرد تنها در درون سلولهای سرطانی – رایجترین رویکرد – لزوماً بهترین راه برای توسعه درمانهای ضد سرطان نیست.
او و همکارانش دریافتند که BACH1 که در بسیاری از اشکال سرطان متاستاتیک مانند ریه و سینه به شدت بیان میشود، میتواند هم فعال یا هم مهارکننده تهاجم سلولهای سرطانی در سلولهای سرطان پستان سهگانه منفی در کشت باشد.
Balázsi، هنری، خلاصه میکند: «ما یک خط لوله فنآوری دو مرحلهای ایجاد کردیم که نوعی «صفحه فرود» ایجاد میکند که در آن ژنهای BACH1 یا دیگر ژنها را میتوان با خیال راحت به هر رده سلولی انسانی وارد کرد، مانند دری که به سمت کلید درست باز میشود. پروفسور لاوفر در مرکز زیست شناسی فیزیکی و کمی لوفر و بئاتریس لافر و استاد مهندسی زیست پزشکی در دانشگاه استونی بروک.
این تیم از راههای مختلفی از جمله CRISPR برای دستکاری ژنتیکی سلولها و ایجاد «سکوی فرود» برای تکمیل مرحله اول استفاده کردند. مرحله دوم شامل توسعه مدارهای ژن مصنوعی برای کنترل مقدار پروتئین بود. این مدارها آنها را قادر میسازد تا از یک «سوئیچ دیمر» استفاده کنند که میزان یا درصد BACH1 قرار داده شده در سلولهای سرطانی را کنترل میکند.
“این کار را مانند یک کلید چراغ در نظر بگیرید، هرچند که نه تنها در “روشن” و “خاموش”، بلکه با ظرفیت کم نور پیچیده کار می کند. بالازی توضیح می دهد که فعال کردن) یا خاموش کردن (مهار)، یک دیمر تنظیم شده داریم که می توانیم مقدار فعال کننده متاستاتیک را از طریق سکوی سکوی فرود به درصدهای متوسط تنظیم کنیم.”
چیزی که محققان را در آزمایش BACH1 در مدل تهاجم به سلول سرطانی شگفت زده کرد این است که کاهش سطح پروتئین همیشه فرآیندهای متاستاتیک را مهار نمی کند و افزایش آن همیشه تهاجم به سلول های سرطانی را افزایش نمی دهد.
آنها می نویسند، “به طور غیرمنتظره ای، سلول های متاستاتیک سینه انسان مهندسی شده MDA-MB-231 با تنظیم سطح BACH1 بدون توجه به BACH1 بومی، بیشتر، سپس کمتر و سپس تهاجمی تر می شوند. بیان BACH1 در سلول های مهاجم تغییر می کند و بیان رونویسی BACH1 تغییر می کند. اهداف، فنوتیپ غیر یکنواخت و اثرات تنظیمی BACH1 را تایید می کنند. بنابراین، مهار شیمیایی BACH1 می تواند اثرات ناخواسته ای بر تهاجم داشته باشد.
آنها همچنین دریافتند که شماره گیری بخشی از BACH1 به یک سطح متوسط، در موقعیت میانی دیمر، در واقع از روند تهاجم سرطان جلوگیری می کند، گویی نور با فشار دادن دکمه دیمر به سمت بالا کمتر می شود.
بالازی میگوید: «یافتههای ما در مورد متاستاز و پروتئینهایی که به نظر میرسد روند سرطان را پیش میبرند، یک داستان احتیاطی ارائه میکنند، یعنی باید نگاه دقیقتری به این پروتئینها و ژنها و نقش دقیق آنها در سرطان بیندازیم.» در برخی موارد ممکن است برای درمان سرطان نیاز به مهار آنها داشته باشیم، و در برخی موارد، بسته به سطح اولیه آنها، باید آنها را افزایش دهیم، یا حتی هر دو، با این حال برای کمک به تعیین هر چیزی قطعی به تحقیقات بیشتری نیاز داریم.
آزمایش آنها نشان داد که با استفاده از تجزیه کننده BACH1، بسته به سطح اصلی BACH1، می تواند تهاجمی سلول های سرطان سینه را کاهش داده یا به طور ناخواسته افزایش دهد. نویسندگان می گویند چنین نتایجی اهمیت مشخص کردن اثرات بیماری ژن ها را با تنظیم سطح پروتئین برجسته می کند.
این تحقیق شامل تیمی از همکاران استونی بروک و سایر موسسات، به ویژه نویسنده اول، دکتر ییمینگ وان بود. کار آنها برای کشف برجسته شده در مقاله ضروری بود.
اطلاعات بیشتر:
Yiming Wan و همکاران، منظره تهاجم غیر یکنواخت با کنترل نویز آگاه سطوح فعال کننده متاستاز، زیست شناسی شیمیایی طبیعت (2023). DOI: 10.1038/s41589-023-01344-z
ارائه شده توسط دانشگاه استونی بروک
نقل قول: بازاندیشی رویکرد بازدارنده پروتئین برای درمان سرطان (2023، 26 مه) در 26 مه 2023 از https://medicalxpress.com/news/2023-05-rethinking-protein-inhibitor-approach-cancer.html بازیابی شده است.
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.
[ad_2]