[ad_1]
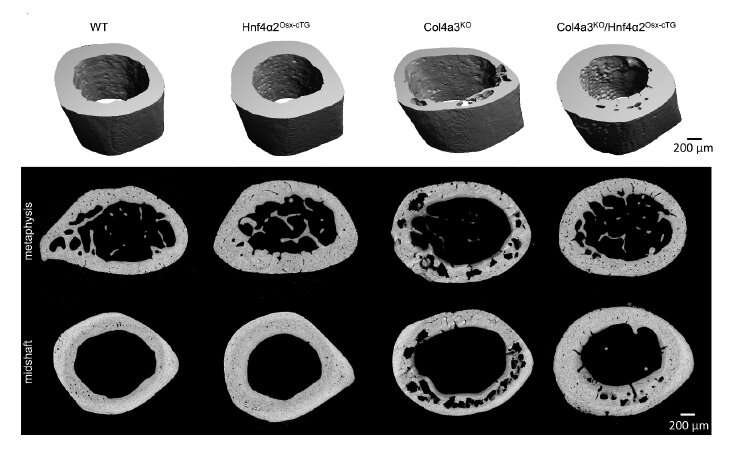
بیان ژنتیکی Hnf4α2 در استئوبلاست ها از تحلیل استخوان در موش های مبتلا به بیماری مزمن کلیوی جلوگیری می کند. تجزیه و تحلیل میکروتوموگرافی استخوان قشر فمور در متافیز و در میانه شفت در موش های نوع وحشی 20 هفته ای. اعتبار: دانشگاه نورث وسترن
بر اساس مطالعهای که اخیراً منتشر شده است، محققان پزشکی Northwestern کشف کردهاند که بیان بیش از حد یک فاکتور رونویسی از تحلیل استخوان در مدلهای موش مبتلا به بیماری مزمن کلیوی جلوگیری میکند. مجله تحقیقات بالینی.
یافتهها نشان میدهد که فاکتور رونویسی فاکتور هستهای هپاتوسیت 4 آلفا (HNF4α) شکنندگی استخوان را تنظیم میکند و در ایجاد استئودیستروفی کلیوی (ROD)، یک عارضه شایع بیماری مزمن کلیوی که متابولیسم سلولهای استخوانی را کاهش میدهد و استخوانها را در طول زمان ضعیف میکند، نقش دارد.
نیکولای والنتین دیوید، دکترای دکتر، فرانک کروملوفسکی، پروفسور پزشکی در بخش نفرولوژی و فشار خون و نویسنده ارشد این مقاله گفت: «این دستنوشته الگویی برای اکتشافات جدید ارائه میکند که میتواند به حل مکانیسمهای اساسی ROD کمک کند. مطالعه.
بیش از 37 میلیون نفر در ایالات متحده به بیماری مزمن کلیوی مبتلا هستند و بیشتر آنها نیز به ROD مبتلا خواهند شد. هیچ درمانی برای این بیماری به جز پیوند کلیه وجود ندارد و عوارض جانبی می تواند شامل از دست دادن استخوان، بدشکلی های اسکلتی، افزایش خطر شکستگی استخوان و مشکلات قلبی عروقی باشد.
در حال حاضر، درمانهای ROD بر درمان اختلال متابولیسم مواد معدنی سیستمیک تمرکز دارد که شامل اصلاح فسفات در گردش، هورمون پاراتیروئید و سطوح ویتامین D است. به گفته دیوید، با وجود این و سایر درمانهای کنونی، شکستگیهای استخوانی مرتبط با بیماری مزمن کلیوی در بیماران بزرگسال و کودکان در دو دهه گذشته بیش از دو برابر شده است که دلیل آن عدم انجام تحقیقات پاتوژنز ROD است.
به گفته والنتین، سیستم طبقهبندی استخوان «تحول، کانیسازی، حجم» (TMV) که برای تعریف نوع ROD استفاده میشود، این موضوع را منعکس میکند. او گفت، با این حال، درک فعلی و محدود پاتوبیولوژی ROD، وضعیت بیشتر علم در زیست شناسی اسکلتی را به طور کلی و در درک سیگنال دهی سلول های استخوانی نشان نمی دهد.
والنتین گفت: «عدم پیشرفت در بهبود نتایج بالینی ROD علیرغم استراتژیهایی که طبقهبندی TMV را در نظر میگیرند، از نیاز به درمانهایی حمایت میکند که بر اساس علم پیشرفته در پاتوبیولوژی ROD هستند.
در مطالعه حاضر، آزمایشگاه والنتین نمونههای بافت استخوانی از بیماران سالم و بیماران مبتلا به بیماری مزمن کلیوی و نمونههای بافت استخوانی از مدلهای موش ROD را بررسی کرد. با استفاده از توالی یابی RNA، آنها دریافتند که HNF4α، یک فاکتور رونویسی که در کبد بیان می شود، در استخوان نیز بیان می شود و بیان استخوان HNF4α در بیماران و موش های مبتلا به ROD کاهش می یابد.
در مرحله بعد، محققان HNF4α را در استئوبلاستها (سلولهایی که استخوان میسازند) را در موشهای مبتلا به بیماری مزمن کلیوی بیان کردند و دریافتند که این باعث کاهش شکنندگی استخوان و به طور کلی اصلاح ناهنجاریهای اسکلتی میشود.
آنها با استفاده از تکنیکهای چند omics برای تجزیه و تحلیل بافت استخوان و استئوبلاستهایی که ایزوفرمهای HNF4α را ندارند یا بیش از حد بیان میکنند، دریافتند که ایزوفرم HNF4α2 استخوانزایی، متابولیسم سلولهای استخوانی و مرگ سلولی را تنظیم میکند.
“آنچه در مورد نقش HNF4α2 در استخوان مهم است، عملکرد حفظ شده آن در بین اندام ها و سلول ها، برای تنظیم فعالیت متابولیک و حمل و نقل در استئوبلاست ها است که با نقش آن در سلول های کبدی و سلول های کلیه لوله پروگزیمال و تنظیم ژن های استخوانی خاص استئوبلاست مقایسه می شود. ” دیوید گفت.
به گفته دیوید، یافتهها نشان میدهد که بیماران ROD به طور بالقوه میتوانند از درمانهای جدید با هدف قرار دادن بیان HNF4α برای به تاخیر انداختن پیشرفت شکنندگی استخوان و بهبود کیفیت زندگی بهره ببرند، اما تنها در صورتی که تلاشهای تحقیقاتی بیشتر بر این هدف متمرکز شود.
“روش های پیشرفته در omics به کار رفته در استخوان منجر به پیشرفت های عمده ای در درک ما از پاتوژنز ROD می شود و به توسعه استراتژی های هدفمند، اصلاح کننده بیماری و درمان کمک می کند. این روش های جدید فقط در حال حاضر برای ROD اعمال می شوند، اما دیوید گفت، زیرساخت های اساسی برای توسعه تحقیقات مرتبط بالینی بیمار محور وجود ندارد و مانع از توسعه استراتژی هایی می شود که زندگی بیماران مبتلا به بیماری مزمن کلیوی را بهبود می بخشد.
دیوید افزود که تیم او اکنون در حال بررسی نقش HNF4α2 در استخوان و کلیه و نقش بزرگتر آن در پیشرفت ROD و بیماری مزمن کلیوی است.
دیوید گفت: “ما فکر می کنیم که کاهش پیشرونده آن در استخوان که به موازات پیشرفت بیماری مزمن کلیه است، بخشی از برنامه ریزی مجدد متابولیک چند عضوی بزرگتر است که در صورت پیشگیری، ممکن است نه تنها پیشرفت ROD بلکه کاهش عملکرد کلیه را نیز به تاخیر بیندازد.” .
اطلاعات بیشتر:
مارتا مارتینز-کاله و همکاران، فاکتور رونویسی HNF4α2 باعث تقویت استخوان سازی و جلوگیری از ناهنجاری های استخوانی در موش های مبتلا به استئودیستروفی کلیوی می شود. مجله تحقیقات بالینی (2023). DOI: 10.1172/JCI159928
ارائه شده توسط دانشگاه نورث وسترن
نقل قول: فاکتور رونویسی از شکنندگی استخوان در بیماری مزمن کلیه جلوگیری می کند (2023، 5 ژوئن) بازیابی شده در 6 ژوئن 2023 از https://medicalxpress.com/news/2023-06-transcription-factor-bone-frailty-chronic.html
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.
[ad_2]