اسکن (به رنگ مصنوعی) از مغز یک فرد مبتلا به بیماری آلزایمر.اعتبار: KH Fung/Science Photo Library
یک داروی آزمایشی می تواند پیشرفت بیماری آلزایمر را در افرادی که زمانی که بیماری هنوز در مراحل اولیه است شروع به مصرف آن کنند، کند کند. این دارو، یک آنتی بادی مونوکلونال به نام دونانماب، علائم را بهبود نمی بخشد. اما در میان افرادی که مصرف آن را در مراحل اولیه آلزایمر شروع کردند، 47٪ پس از یک سال هیچ پیشرفت بیماری در برخی اقدامات نداشتند، در حالی که 29٪ دارونما مصرف کردند.
این دارو برای افراد در مراحل بعدی یا افرادی که تنوع ژنتیکی مشترکی دارند که خطر ابتلا به این بیماری را افزایش می دهد، سود چندانی ندارد.
ریسا اسپرلینگ، متخصص مغز و اعصاب در دانشکده پزشکی هاروارد در بوستون، ماساچوست، می گوید که نتایج “بسیار دلگرم کننده” هستند، به ویژه به این دلیل که آنها مشابه داروهای مشابهی به نام lecanemab هستند. این به من این احساس را می دهد که در مسیر درستی هستیم.
سازنده Donanemab، Eli Lilly، مستقر در ایندیاناپولیس، ایندیانا، نتایج آزمایش 1736 نفر را امروز در کنفرانس بین المللی انجمن آلزایمر (AAIC) در آمستردام ارائه و آنها را منتشر کرد.1 که در جاما. این شرکت نتایج جزئی را در ماه مه منتشر کرد، اما محققان هنوز در مورد ایمنی و اثربخشی دارو در گروههای خاص سؤالاتی داشتند.
هدف چسبنده
مانند بسیاری از داروهای دیگر در جدیدترین نسل داروهای آلزایمر، دونانماب یک آنتی بادی مونوکلونال است که آمیلوئید، پروتئین چسبنده و آسیبرسان به نورون را در مغز افراد مبتلا به زوال عقل هدف قرار میدهد. Donanemab، مانند lecanemab و داروی مربوط به aducanumab، میتواند باعث بیماری به نام ناهنجاریهای تصویربرداری مرتبط با آمیلوئید (ARIA) شود که گاهی منجر به خونریزی مغزی و تشنج بالقوه کشنده میشود. حدود یک چهارم شرکت کنندگان در مرحله سوم آزمایش الی لیلی به ARIA مبتلا شدند و سه نفر به دلیل این بیماری جان خود را از دست دادند. ARIA در میان شرکت کنندگان در مطالعه که حامل آن بودند، شایع بود APOE4 تنوع ژنتیکی که خطر ابتلا به آلزایمر را افزایش می دهد.
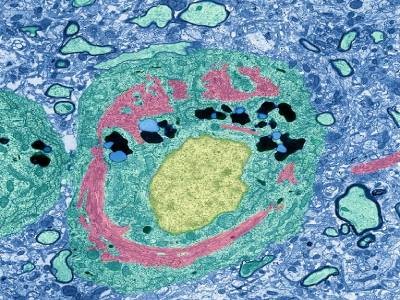
این گونه است که ژن آلزایمر مغز را تخریب می کند
شرکت کنندگان حمل می کنند APOE4 دادههای کامل نشان داد که نسبت به شرکتکنندگانی که این واریته را نداشتند، کمتر از دونانماب بهره بردند. و این دارو در افرادی که زمانی که سطح پروتئین مغز دیگری به نام تاو پایین است، شروع به مصرف آن می کنند، بسیار بهتر عمل می کند. سطح تاو با پیشرفت آلزایمر افزایش می یابد، اگرچه نقش آن در این بیماری هنوز به خوبی شناخته نشده است.
افراد با سطوح کم یا متوسط تاو که دونانماب مصرف کردند، در طول 76 هفته 35 درصد کندتر از افرادی که دارونما مصرف کردند، کاهش یافتند. اما آنهایی که سطح تاو بالایی داشتند، صرف نظر از اینکه دونانماب یا دارونما مصرف کردند، با همان سرعت کاهش یافتند. در یک کنفرانس مطبوعاتی در AAIC، مارک مینتون، معاون تحقیق و توسعه علوم اعصاب در Eli Lilly، گفت که اگرچه توسعه آزمایشهای بهتر برای تعیین سطح تاو مهم است، او فکر نمیکند که پزشکان نیازی به ارزیابی سطح تاو بیمار قبل از تصمیم گیری در مورد تجویز دارو.
کاهش روند کاهشی
در افراد مبتلا به اختلال شناختی نسبتاً جزئی که شروع به مصرف دونانماب کردند، کاهش شناختی تا 60٪ کاهش یافت. این دارو همچنین حدود 90 درصد از مقدار کل آمیلوئید را از مغز پاک کرد. هنگامی که افراد دارای حداقل سطح آمیلوئید بودند، محققان آنها را به دارونما تغییر دادند. در سال پس از تغییر، افرادی که دونانماب مصرف کرده بودند با سرعت کمتری نسبت به افرادی که در ابتدا دارونما دریافت کرده بودند، کاهش یافتند.
اسپرلینگ می گوید، نتایج نشان می دهد که افراد مبتلا به آلزایمر در صورت تشخیص زودهنگام و درمان، نتیجه بهتری خواهند داشت. او خاطرنشان می کند که آزمایشات بالینی در حال آزمایش هستند که آیا lecanemab و donanemab می توانند از این بیماری در افرادی که هنوز علائمی ایجاد نکرده اند جلوگیری کنند.
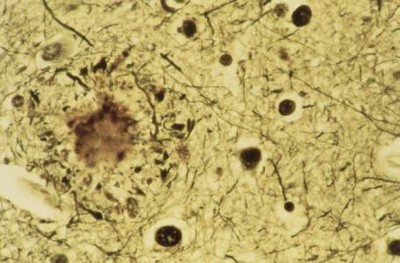
داروی آلزایمر زوال ذهنی را در آزمایش کند می کند – اما آیا این یک پیشرفت است؟
بارت دی استروپر، محقق آلزایمر در دانشگاه کالج لندن می گوید این یافته تاریخی است. همه چیز در این کارآزمایی به ما می گوید که باید از تجمع آمیلوئید جلوگیری کنیم. اما دی استروپر می افزاید که این دارو فقط بر روی افرادی با نشانگرهای بیولوژیکی خاص آلزایمر آزمایش شده است و ممکن است در دیگران موثر نباشد.
برنت فارستر، روانپزشک سالمندان در دانشکده پزشکی دانشگاه تافتس در بوستون، ماساچوست، نگران این است که چگونه دونانماب و سایر داروها در عمل بالینی کار خواهند کرد. به عنوان مثال، مشخص نیست که آیا پزشکان باید طرح آزمایشی را کپی کنند و زمانی که افراد دیگر آمیلوئید در مغزشان وجود نداشت، دارو را کنار بگذارند. او میگوید که غربالگری ARIA احتمالاً گران و دشوار خواهد بود، و همچنین شناسایی افرادی که به احتمال زیاد از درمان سود میبرند.
در این کنفرانس مطبوعاتی، جان سیمز، مدیر ارشد پزشکی Eli Lilly گفت که این شرکت برای تایید سازمان غذا و داروی ایالات متحده ثبت نام کرده است و انتظار دارد تا پایان سال پاسخ دهد.
Sims و Mintun از اظهار نظر در مورد هزینه دونانماب در صورت تایید خودداری کردند، اما lecanemab و aducanumab بیش از 26000 دلار آمریکا در سال قیمت گذاری شده اند.