[ad_1]
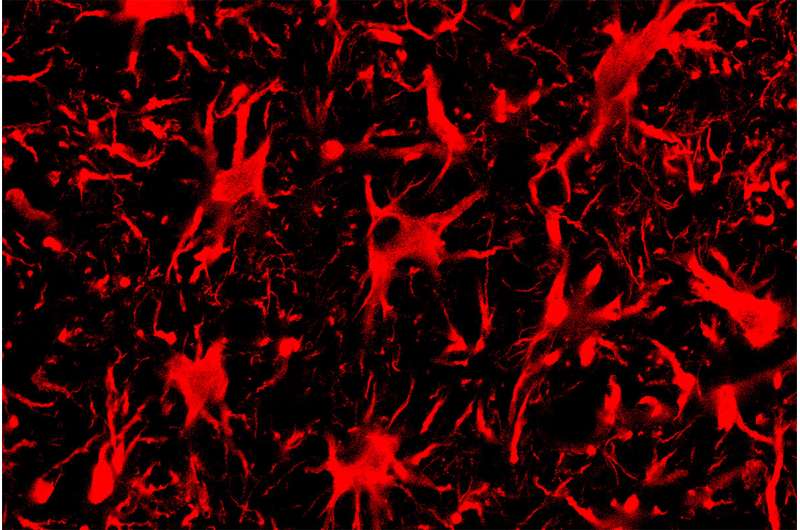
آستروسیت های نخاعی، سلول هایی که در این تصویر میکروسکوپ فلورسنت دیده می شوند، در پیشرفت ALS نقش دارند. یک سیستم جدید CRISPR-Cas13 که تولید پروتئین جهش یافته در این سلول ها را هدف قرار می دهد، نتایج را برای موش های مبتلا به ALS بهبود بخشید. اعتبار: توماس گاج و کالین لیم
یک جهش ژنتیکی می تواند عواقب عمیقی داشته باشد، همانطور که در بیماری های نورودژنراتیو مانند اسکلروز جانبی آمیوتروفیک یا بیماری هانتینگتون نشان داده شده است. مطالعه جدیدی که توسط محققان دانشگاه ایلینویز Urbana-Champaign انجام شد، از روش هدفمند CRISPR در سیستم عصبی مرکزی موشها برای جلوگیری از تولید پروتئینهای جهشیافته که میتوانند باعث ALS و بیماری هانتینگتون شوند، استفاده کردند.
به جای تکنیک محبوب ویرایش DNA CRISPR-Cas9، رویکرد جدید از CRISPR-Cas13 استفاده میکند که میتواند mRNA را هدف قرار دهد – مولکول پیامرسانی که نقشههای پروتئینی رونویسی شده از DNA را حمل میکند. توماس گاج، سرپرست این مطالعه، پروفسور مهندسی زیستی ایلینویز، گفت که تیم ایلینوی سیستمهای Cas13 را برای هدفگیری و برش RNAهایی که پروتئینهای جهشیافته را که باعث ALS و بیماری هانتینگتون میشوند، کد میکنند، توسعه دادند و به طور مؤثر ژنهای جهشیافته را بدون ایجاد اختلال در DNA سلول خاموش میکنند. این تیم نتایج خود را در مجله منتشر کرد پیشرفت علم.
کالین لیم، دانشجوی فارغ التحصیل که به رهبری این مطالعه کمک کرد، گفت: “RNA هدف به جای DNA دارای مزایای منحصر به فردی است، از جمله این واقعیت که در تئوری، اثرات آن در سلول می تواند معکوس شود، زیرا RNA ها مولکول های گذرا هستند.” از آنجایی که آنزیمهای Cas13 فقط RNA را هدف قرار میدهند، حداقل خطر را برای ایجاد هرگونه جهش دائمی خارج از هدف به DNA دارند.
محققان سیستم های CRISPR-Cas13 را به سیستم عصبی مرکزی موش های دارای جهش ژنتیکی که باعث بیماری ALS یا هانتینگتون می شود، تزریق کردند. ناقلهای ویروس مرتبط با آدنو، سیستمهای هدفگیری RNA را به سلولها منتقل کردند. گاج گفت که این ناقل ها وسیله ای امیدوارکننده برای ژن درمانی هستند تا حدی به دلیل توانایی آنها برای ورود به سلول های نخاع و مغز.
محققان دریافتند که CRISPR-Cas13 به طور موثر میزان پروتئین جهش یافته موجود در سیستم عصبی را برای هر دو بیماری کاهش می دهد – به ویژه پروتئین SOD1 در نخاع موش های مبتلا به ALS و پروتئین “huntingtin” در مغز موش های مبتلا به هانتینگتون. مرض. کاهش پروتئین SOD1 جهش یافته نیز با نتایج درمانی بهتر مرتبط است: موشهای مبتلا به ALS که تزریق CRISPR-Cas13 را دریافت کردند، در مقایسه با موشهایی که تزریق CRISPR-Cas13 را دریافت کردند، پیشرفت کندتر بیماری، بهبود بقا و کاهش سرعت پایینتری در قدرت گرفتن و مهارتهای حرکتی داشتند. رفتار.
محققان گفتند این مطالعه شواهد مهمی را ارائه میکند که نشان میدهد CRISPR-Cas13 میتواند ژنهای هدف را در سیستم عصبی از بین ببرد، که گامی کلیدی به سوی توسعه درمانهای هدفمند بر اساس این فناوری است. با این حال، آنها گفتند که مطالعات بیشتری برای درک بهتر نحوه عملکرد Cas13، یک آنزیم باکتریایی در سلولهای پستانداران، به ویژه اینکه آیا میتواند توالیهای RNA ناخواسته را هدف قرار دهد یا باعث پاسخهای ایمنی شود، مورد نیاز است.
گاج گفت: «در آزمایشهای ما، Cas13 به طور کلی به اندازه روشهای خاموشکننده ژنی مشخص بود که در کنار آن آزمایش کردیم. “اما تعیین اینکه Cas13 دقیقا چقدر خاص و در نتیجه چقدر ایمن است در سلول های انسانی یک سوال مهم برای این زمینه باقی مانده است.
“ما در مورد بررسی پتانسیل Cas13 و دیگر آنزیم های CRISPR هدف گیری RNA هیجان زده هستیم. با این حال، این فناوری هنوز در مراحل ابتدایی خود است. بسیاری از سوالات مهم در مورد ویژگی آن و توانایی آن در جدا کردن RNA های غیرهدف باید پاسخ داده شود، که همه آنها پاسخ خواهند داد. به اصلاح و استفاده آتی آن کمک کند.”
سیستم فشرده CRISPR آزمایش کووید-19 قابل حمل را امکان پذیر می کند
جکسون ای. پاول و همکاران، خاموش کردن ژن هدفمند در سیستم عصبی با CRISPR-Cas13، پیشرفت علم (2022). DOI: 10.1126/sciadv.abk2485
ارائه شده توسط دانشگاه ایلینوی در Urbana-Champaign
نقل قول: تکنیک CRISPR-Cas13 پروتئین های عامل ALS و بیماری هانتینگتون را در سیستم عصبی موش هدف قرار می دهد (2022، 19 ژانویه) در 19 ژانویه 2022 از https://medicalxpress.com/news/2022-01-crispr-cas13-technique-proteins- بازیابی شده است. als-huntington.html
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.
[ad_2]