[ad_1]
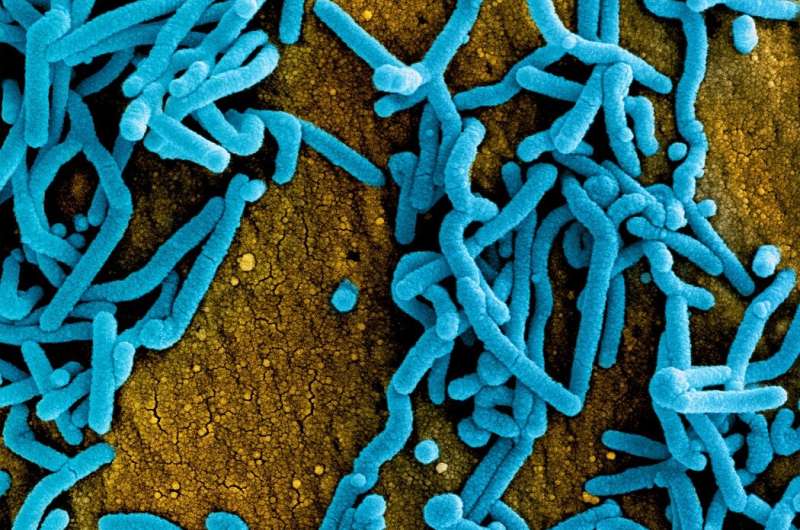
میکروگراف الکترونی روبشی رنگی ذرات ویروس ماربورگ (آبی) هم جوانه زده و هم به سطح سلول های VERO E6 آلوده (نارنجی) متصل شده اند. اعتبار: NIAID
مقاله تازه منتشر شده در لانست نشان میدهد که یک واکسن آزمایشی علیه ویروس ماربورگ (MARV) بیخطر بوده و در یک کارآزمایی بالینی کوچک و برای اولین بار در انسان باعث ایجاد پاسخ ایمنی میشود. این واکسن که توسط محققان موسسه ملی آلرژی و بیماریهای عفونی (NIAID) که بخشی از موسسه ملی بهداشت است، ساخته شده است، میتواند روزی ابزار مهمی برای پاسخ به شیوع ویروس ماربورگ باشد.
این مطالعه برای اولین بار در انسان، فاز 1، یک کاندید آزمایشی واکسن MARV، معروف به cAd3-Marburg را آزمایش کرد که در مرکز تحقیقات واکسن NIAID (VRC) توسعه یافته بود. این واکسن از یک آدنوویروس شامپانزه اصلاح شده به نام cAd3 استفاده می کند که دیگر نمی تواند تکثیر یا سلول ها را آلوده کند و گلیکوپروتئین موجود در سطح MARV را برای القای پاسخ های ایمنی در برابر ویروس نمایش می دهد. پلتفرم واکسن cAd3 در آزمایشهای بالینی قبلی، هنگامی که در واکسنهای تحقیقاتی ویروس ابولا و ویروس سودان که توسط VRC تولید شدهاند، استفاده میشود، مشخصات ایمنی خوبی را نشان داد.
MARV، یک فیلوویروس از خانواده ویروس ابولا، باعث یک بیماری تب دار به سرعت پیشرونده می شود که منجر به شوک و مرگ در بخش بزرگی از افراد آلوده می شود. بسیاری از دانشمندان فکر میکنند که شیوع بیماری MARV در انسان زمانی آغاز میشود که ویروس از میزبان حیوانی اصلی خود که احتمالاً خفاشهای آلوده مزمن در جنوب صحرای آفریقا هستند، پرش کند. علائم بیماری MARV شبیه علائمی است که در بیماری ویروس ابولا مشاهده می شود و می تواند شامل تب، سردرد، لرز، بثورات پوستی، درد شکم، استفراغ و اسهال باشد. با پیشرفت بیماری، بیماران ممکن است از اختلال عملکرد ارگان های متعدد، هذیان، و خونریزی قابل توجهی از دستگاه گوارش یا سایر نقاط که ممکن است منجر به مرگ شود، رنج ببرند.
هیچ واکسن تایید شده یا درمان خاصی برای بیماری MARV به غیر از مراقبت های حمایتی موجود نیست. در حالی که برخی از واکسنهای آزمایشی قبلاً آزمایش شدهاند، هیچکدام ثابت نکردهاند که هم بسیار مؤثر بوده و هم محافظت بادوام را ارائه میکنند. در مناطقی از آفریقا که واکسن ماربورگ بیشتر مورد نیاز است، یک واکسن تک دوز که بتواند در مدت طولانی از گیرندگان محافظت کند، بخش مهمی از سرکوب شیوع بیماری خواهد بود.
در این مطالعه، 40 داوطلب بالغ سالم در مرکز تحقیقات بالینی موسسه تحقیقاتی ارتش والتر رید در سیلور اسپرینگ، مریلند ثبت نام کردند. آنها یک دوز واحد از دوز پایین واکسن (1×10) دریافت کردند10 واحد ذرات) یا دوز بالاتر (1×1011 واحدهای ذرات). برای ایمنی، داوطلبان در یک طرح افزایش دوز ثبت نام شدند. سه شرکت کننده دوز کمتری را دریافت کردند. سپس، هنگامی که آنها پس از هفت روز اول واکنش های نامطلوب شدیدی را نشان ندادند، کارآزمایی برای ثبت نام 17 داوطلب باقی مانده آغاز شد. از همین روش برای گروه دوز بالاتر نیز استفاده شد. داوطلبان از نظر واکنش های نامطلوب به واکسن مورد بررسی قرار گرفتند و در فواصل منظم به مدت 48 هفته برای ردیابی پاسخ های ایمنی آنها مورد ارزیابی قرار گرفتند.
نتایج ایمنی کارآزمایی دلگرم کننده بود: هیچ عارضه جانبی جدی وجود نداشت و واکسن تجربی به خوبی تحمل شد. یکی از شرکتکنندگان در گروه دوز بالاتر به دنبال واکسیناسیون تب داشت، اما تا روز بعد برطرف شد. علاوه بر این، به نظر میرسد واکسن تحقیقاتی ایمنی قوی و طولانیمدتی را نسبت به گلیکوپروتئین MARV ایجاد میکند: 95 درصد شرکتکنندگان در کارآزمایی پس از واکسیناسیون پاسخ آنتیبادی قوی نشان دادند و 70 درصد آن پاسخ را برای بیش از 48 هفته حفظ کردند.
برنامه هایی برای انجام آزمایشات بیشتر واکسن cAd3-Marburg در غنا، کنیا، اوگاندا و ایالات متحده در دست اجرا است. اگر دادههای اضافی از نتایج امیدوارکنندهای که در آزمایش فاز 1 دیده میشود پشتیبانی کند، واکسن ویروس cAd3-Marburg میتواند روزی در واکنشهای اضطراری به شیوع MARV استفاده شود.
اطلاعات بیشتر:
ملیندا جی هامر و همکاران، ایمنی، تحمل و ایمنی زایی واکسن آدنوویروس ماربورگ نوع 3 ناقل شامپانزه (cAd3-Marburg) در بزرگسالان سالم در ایالات متحده: اولین در انسان، فاز 1، دوز با برچسب باز -آزمایش تشدید، لانست (2023). DOI: 10.1016/S0140-6736(22)02400-X
ارائه شده توسط NIH / موسسه ملی آلرژی و بیماری های عفونی
نقل قول: واکسن ویروس ماربورگ نتایج امیدوارکنندهای را در مطالعه اولین در انسان نشان میدهد (2023، 30 ژانویه) که در 30 ژانویه 2023 از https://medicalxpress.com/news/2023-01-marburg-virus-vaccine-results-first-in بازیابی شد. -human.html
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.
[ad_2]