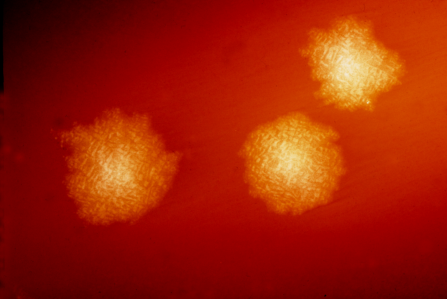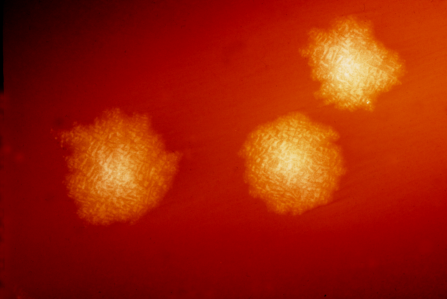
این عکس کلونی های کلستریدیوم دیفیسیل را پس از 48 ساعت رشد روی صفحه خون آگار نشان می دهد. دیفیسیل بزرگ 4.8XC، یک میله گرم مثبت بی هوازی، شایع ترین علت شناسایی شده اسهال مرتبط با آنتی بیوتیک (AAD) است. تقریباً 15-25٪ از تمام قسمت های AAD را تشکیل می دهد. اعتبار: CDC
دانشمندان در سراسر جهان به طور جدی برای بهبود درک یک ابر میکروب خطرناک، کلستریدیوم دیفیسیل، کار کردهاند. پاتوژن بسیار مسری اکتسابی از بیمارستان، که توسط مراکز کنترل و پیشگیری از بیماری ها به عنوان یکی از پنج تهدید فوری برای سیستم مراقبت های بهداشتی ایالات متحده تعیین شده است، هر ساله باعث بیش از 500000 عفونت و 29000 مرگ و میر با مجموع هزینه های اجتماعی بیش از 5 میلیارد دلار می شود.
زیستشناسان دانشگاه A&M تگزاس و کالج پزشکی بیلور در یک مطالعه جدید زیستشناسی سیستمهای با بودجه مؤسسه ملی سلامت با هدف مقابله با مشکل در منبع آن – نقطه اولیه عفونت – با هم همکاری کردهاند، به این امید که مشخص کنند چه چیزی بیماران را مستعد ابتلا به آن میکند. در وهله اول.
مطالعات قبلی نشان داده است که عفونت C. difficile با فراوانی بالای اسیدهای صفراوی ثانویه که برای C. difficile در محیط های آزمایشگاهی سمی هستند، ارتباط قوی دارد. این مولکول های کوچک توسط یک میکروبیوم روده سالم از اسیدهای صفراوی اولیه که در کبد سنتز می شوند، تولید می شوند.
زیستشناس تگزاس A&M و همکار EDGES 2020 جوزف سورگ میگوید که دانشمندان مدتهاست که این مولکولهای کوچک را به عنوان محافظی کلیدی در جلوگیری از عفونت C. difficile میدانند. این تحقیق برای اولین بار توسط دانشجوی فارغ التحصیل آزمایشگاه سورگ آندریا مارتینز آگویر در مقاله ای که اوایل پاییز امسال در مجله منتشر شد، ارائه شد. پاتوژن های PLOS با کمک گروه تور ساویدج در کالج پزشکی بیلور.
سورگ گفت: «تعداد زیادی در حال توسعه گزینههای درمانی پروبیوتیک برای بیماران مبتلا به C. diff هستند – تلاشهایی که بر بازگرداندن اسیدهای صفراوی ثانویه به بیماران متمرکز است.» یافتههای ما نشان میدهد که این درمانها باید به جای آن بر میکروبهایی تمرکز کنند که مواد مغذی مهم برای رشد C. diff را مصرف میکنند و اینکه اسیدهای صفراوی ثانویه برای محافظت از شاه ماهی قرمز هستند.
به عنوان مبنای مطالعه خود، این تیم از موشهای بدون میکروب در کالج پزشکی Baylor استفاده کردند که با یک گونه باکتری شناخته شده در تولید اسید صفراوی ثانویه مستعمره شده بودند و به شدت با محیط محافظ C. difficile همبستگی داشتند. به عنوان یک اقدام کنترلی اضافی، آنها یک سویه موش جهش یافته خریداری شده از طریق پروژه موش ناک اوت NIH را انتخاب کردند که در تگزاس A&M پرورش یافته بود و به دلیل ناتوانی آن در سنتز یک کلاس اصلی از اسیدهای صفراوی متمایز بود، در نتیجه مخزن اسید صفراوی ثانویه را محدودتر کرد.
سورگ گفت: «در کمال تعجب متوجه شدیم که موشهای مستعمره با این میکروبها (C. scindens، C. hiranonis یا C. leptum) در برابر بیماری C. diff محافظت میکنند اما اسیدهای صفراوی ثانویه تولید نمیکنند.
سورگ در سال 2010 به دپارتمان زیست شناسی A&M تگزاس پیوست و از دوران فوق دکتری خود برای بازگشایی علوم پایه C. difficile، از فیزیولوژی تا بیماری زای آن، کار کرده است. او در سال 2006، در همان سالی که ژنوم C. difficile توالی یابی شد، دکترای میکروبیولوژی خود را در دانشگاه شیکاگو دریافت کرد و از آن زمان به عنوان یکی از پیشگامان مطالعه C. difficile ظاهر شد.
آنتی بیوتیک ها با از بین بردن باکتری های تغییر دهنده اسید صفراوی راه را برای عفونت های C. diff هموار می کنند
Andrea Martinez Aguirre و همکاران، محافظت مستقل از اسید صفراوی در برابر عفونت Clostridioides difficile، پاتوژن های PLOS (2021). DOI: 10.1371/journal.ppat.1010015
ارائه شده توسط دانشگاه A&M تگزاس
نقل قول: محققان بر روی «سوپرباگ» تهدیدکننده تمرکز میکنند، به این امید که تشخیص دهند چه چیزی بیماران را مستعد میکند (2021، 2 دسامبر) در 2 دسامبر 2021 از https://medicalxpress.com/news/2021-12-focus-menacing-superbug-patients-susceptible بازیابی شده است. .html
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.