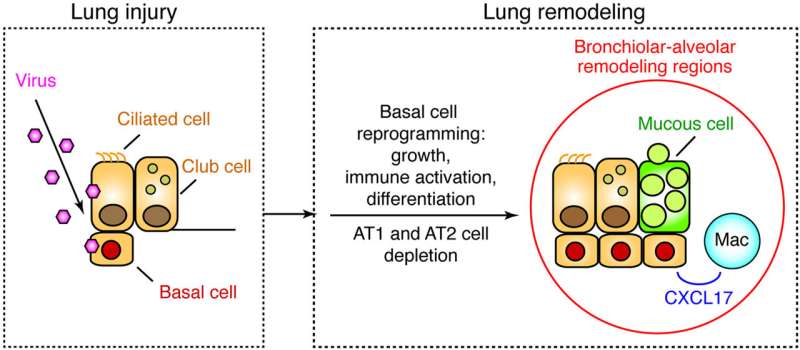
نتایج نشان میدهد که یک فرآیند بازسازی ریه برونشیولار-آلوئولار است که با i) هیپرپلازی سلولهای اپیتلیال پایه و متاپلازی با گسترش به فضاهای آلوئولی سابق مشخص میشود. ii) تخلیه کلوکالیزه انواع آلوئولی سلول های اپیتلیال که به طور معمول در این فضاها یافت می شوند. iii) تمایز سلول های پیش ساز بنیادی اپیتلیال به سلول های مخاطی با موسین های مشخصه مکان های مخاطی و زیر مخاطی. و IV) تولید سلول های اپیتلیال پایه کموکاین CXCL17 مرتبط با ارتشاح ریه مونوسیت-ماکروفاژ. اعتبار: “نواحی بازسازی ریه در بیماری طولانی مدت کروناویروس 19 با برنامه ریزی مجدد سلول های اپیتلیال پایه” توسط کانگیون وو و همکاران، مجله آمریکایی آسیب شناسی
مطالعات اولیه COVID-19 بر مرحله حاد بیماری متمرکز بود. با این حال، در حال حاضر توجه به پیامدهای درازمدت این بیماری معطوف شده است، که همچنین از علل مهم عوارض و مرگ و میر هستند.
دو مطالعه گزارش شده در مجله آمریکایی آسیب شناسی به دنبال درک محرک های مرحله مزمن و گاه پیشرونده بیماری و شناسایی مسیرهای احتمالی برای درمان دارویی هستند.
همهگیری COVID-19 نیاز به درک بهتر بیماریهای حاد و مزمن ناشی از عفونت ویروسی شدید تنفسی را برجسته کرده است. مرحله حاد بیماری با پنومونی شدید و آسیب ریه بر تلاشهای مدیریت اولیه و اولویتهای تحقیقاتی تسلط داشت. با این حال، بیماری پیشرونده و اغلب طولانی مدت نیز یکی از علل مهم عوارض و مرگ و میر است.
درصد بالایی از بیماران مبتلا به کووید-19 از بیماری عفونی حاد جان سالم به در بردند تا درجه قابل توجهی از اختلال عملکرد اندام را در مدت طولانیتری در طول بستری شدن اولیه و پس از آن تجربه کنند.
در اولین مطالعه ای که در اینجا برجسته شده است، محققین یک نقشه راه برای پاتوژنز بیماری ریه پس از ویروسی و مبنایی برای درمان دارویی برای COVID-19 طولانی مدت و شرایط پس از ویروسی مرتبط ارائه می دهند. در مطالعه دوم، محققان از یک مدل همستر از COVID-19 انسانی برای مطالعه علت ناهنجاریهای انعقادی و شاخصهای میکروسکوپی آسیب عروق ریوی مرتبط با موارد شدید COVID-19 در انسان استفاده کردند.
نتایج نشان داد که آسیب عروقی غیرمستقیم، احتمالاً ثانویه به اختلال عملکرد سیستم ایمنی، یکی از عوامل اصلی آسیب عروقی است، که نشان میدهد که درمانهای جدید که سیستم ایمنی نامنظم را هدف قرار میدهند ممکن است مؤثر واقع شوند.
در مطالعه ای که توسط مایکل جی. هولتزمن، MD، پزشکی ریوی و مراقبت های ویژه، گروه پزشکی، و گروه زیست شناسی و فیزیولوژی سلولی، دانشکده پزشکی دانشگاه واشنگتن، سنت لوئیس، انجام شد، محققان مجموعه ای از کالبد شکافی های بیماران را که مدت ها پس از آن انجام شد، بررسی کردند. شروع COVID-19.
دکتر هولتزمن توضیح داد: “تحقیقات ما الهام گرفته از نیاز مبرم به درک بحران COVID-19، و به ویژه برای تعریف علت بیماری بود. ما یک سری موارد مرگبار متوالی را که بین 27 تا 51 روز پس از کالبد شکافی انجام شد، بررسی کردیم. بستری شدن در بیمارستان. در هر بیمار، ما یک الگوی کلیشهای برونشیولار-آلوئولار از بازسازی ریه را با هیپرپلازی سلولهای اپیتلیال پایه، فعالسازی ایمنی و تمایز موسینوس شناسایی کردیم.
نواحی بازسازی شده همچنین دارای انفیلتراسیون ماکروفاژها و آپوپتوز و کاهش مشخص سلول های اپیتلیال آلوئولی نوع 1 و 2 بودند. این الگو بسیار شبیه به مدل های تجربی ما از بیماری پیشرونده ریه پس از عفونت ویروسی تنفسی بود.
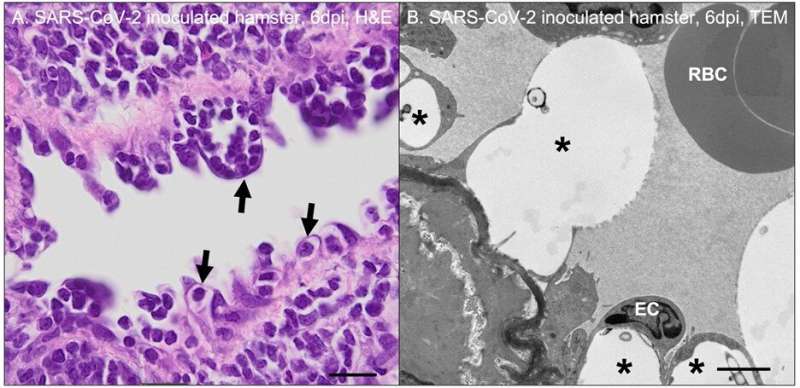
(الف) بخش بافت ریه از یک همستر تلقیح شده با SARS-CoV-2 که معدوم شده است (6 روز پس از عفونت (dpi). اندوتلییت تک هسته ای برجسته (پیکان) همراه با التهاب اطراف عروقی وجود دارد. رنگ آمیزی هماتوکسیلین و ائوزین (H&E) (اعتبار: Erin Ball) با اسکن اسلاید توسط M. Kevin Keel). (B) تصاویر میکروسکوپ الکترونی عبوری (TEM) از رگ خونی ریوی همستر شش روز پس از تلقیح با SARS-CoV-2. سلولهای اندوتلیال (EC) آسیبدیده با سیتوپلاسمی مشخص وجود دارد. واکوئلاسیون (ستاره ها). RBC = گلبول قرمز؛ نوار مقیاس (A) = 20 میکرومتر؛ نوار مقیاس (B) = 2 میکرومتر. اعتبار: بردلی شیباتا، “واسکولوپاتی سندرم تنفسی حاد کروناویروس 2 در مدل همستر طلایی سوریه،” توسط Erin E. Ball و همکاران، مجله آمریکایی آسیب شناسی
محققان چندین تأثیر علمی کلیدی را بر اساس شناسایی نواحی بازسازیکننده با هیپرپلازی سلولهای اپیتلیال پایه و متاپلازی که به فضاهای آلوئولی سابق گسترش مییابد، اشاره کردند. ریزش همزمان هر دو نوع سلول اپیتلیال آلوئولی که به طور معمول در این فضاها یافت می شود. تمایز سلول های بنیادی- پیش ساز اپیتلیال به سلول های مخاطی با مخلوطی از انواع مخاطی و زیر مخاطی تولید موسین. و نفوذ ماکروفاژ به تولید کموکاین سلول های اپیتلیال پایه مرتبط است.
دکتر هولتزمن اظهار داشت: «این مطالعات همراه با نتایج مدلهای حیوانی منتشر شده قبلی ما از بیماری ریه پس از ویروسی، نقشه راهی برای پاتوژنز بیماری ریوی پس از ویروسی و مبنایی برای استراتژی اصلاح بیماری برای طولانی مدت ارائه میدهند. اصطلاح COVID-19 و شرایط پس از ویروسی مرتبط. این تحقیق یک الگوی بیماری را تعریف میکند که اهداف سلولی و مولکولی خاصی را برای درمان در بر میگیرد. در واقع، ما اکنون در حال توسعه درمانی دارویی هستیم که دقیقاً هدف آن رفع آن اهداف است.”
با پیشرفت همهگیری، پزشکان مکرراً شواهد بالینی ناهنجاریهای انعقادی و شاخصهای میکروسکوپی آسیب عروق ریوی مرتبط با موارد شدید انسانی COVID-19 را گزارش کردند، Erin E. Ball، DVM، Ph.D.، بخش پاتولوژی، میکروبیولوژی و اشاره کرد. ایمونولوژی، دانشگاه کالیفرنیا، دیویس، و همکاران.
تیمی از محققین به سرپرستی دکتر بال، سندرم حاد تنفسی ویروس کرونا 2 (SARS-CoV-2) را که باعث COVID-19 میشود به یک مدل همستر طلایی سوری از COVID-19 انسانی تزریق کردند تا علت آسیب عروق ریوی را تعیین کنند. سه تا هفت روز پس از تلقیح، آن ها آنتی ژن و RNA SARS-CoV-2 را در سلول های اپیتلیال راه هوایی، پنوموسیت ها و ماکروفاژها شناسایی کردند، اما با رگ های خونی مرتبط نبودند.
نتایج آنها نشان داد که مناطق التهاب ریوی فعال در عفونت SARS-CoV-2 با شواهد فراساختاری آسیب اندوتلیال همراه با حاشیهسازی پلاکتها و انفیلتراسیون ماکروفاژهای اطراف عروقی و ساب اندوتلیال مشخص میشوند. آنتی ژن یا RNA SARS-CoV-2 در رگ های خونی مبتلا قابل تشخیص نبود.
محققان در ابتدا تصور می کردند ضایعات عروقی میکروسکوپی برجسته که در همسترها بین سه تا هفت روز پس از تلقیح SARS-CoV-2 مشاهده می شود، نتیجه عفونت مستقیم ویروسی سلول های متشکل از رگ های خونی است. با این حال، این مورد نبود.
دکتر بال افزود: “این یافتهها نشان میدهد که آسیب غیرمستقیم عروقی، احتمالاً ثانویه به اختلال عملکرد سیستم ایمنی، عامل اصلی آسیب عروقی مشاهدهشده در همسترهای تلقیحشده با SARS-CoV-2 و عفونت بالقوه شدید COVID-19 در انسان است. اختلال در تنظیم ایمنی ناشی از آن. در تولید بیش از حد سیتوکین های پیش التهابی، آسیب اندوتلیال و بیش فعال شدن پلاکت ها یک نیروی محرکه قابل قبول در پشت حالت هیپرانعقاد و میکروترومبوز مشاهده شده در برخی از بیماران COVID-19 است.
اگرچه این یک مطالعه مشاهدهای بود، این یافتهها و بهویژه عدم ارتباط ویروسی با رگهای ملتهب همراه با دادههای منتشر شده، در مجموع از مکانیسم غیرمستقیم مرتبط با التهاب و انعقاد بیش از حد در موارد شدید COVID-19 پشتیبانی میکنند. این نتایج نشان میدهد که درمانهای جدید که سیستم ایمنی نامنظم را هدف قرار میدهند، ممکن است اقدامات متقابل پزشکی مؤثری در برابر COVID-19 ثابت کنند.
اطلاعات بیشتر:
کانگیون وو و همکاران، مناطق بازسازی ریه در بیماری کروناویروس درازمدت 2019 ویژگی برنامهریزی مجدد سلولهای اپیتلیال پایه، مجله آمریکایی آسیب شناسی (2023). DOI: 10.1016/j.ajpath.2023.02.005
ارین ای. بال و همکاران، واسکولوپاتی سندرم حاد تنفسی کروناویروس 2 در مدل همستر طلایی سوریه، مجله آمریکایی آسیب شناسی (2023). DOI: 10.1016/j.ajpath.2023.02.013
نقل قول: دو مطالعه جدید مسیرهای امیدوارکننده ای را برای درمان کووید-19 مزمن شناسایی می کنند (2023، 6 ژوئن) که در 6 ژوئن 2023 از https://medicalxpress.com/news/2023-06-pathways-chronic-covid-.html بازیابی شده است.
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.
