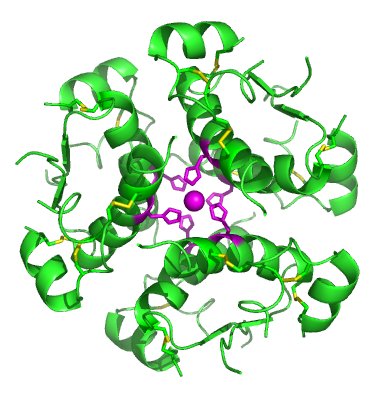
مدل با وضوح بالا از شش مولکول انسولین مونتاژ شده در یک هگزامر. اعتبار: ایزاک یونموتو/ویکی پدیا
نتایج موقت از یک کارآزمایی بالینی چند مرکزی، ترشح انسولین از سلولهای پیوند شده را در بیماران مبتلا به دیابت نوع 1 نشان میدهد. ایمنی، تحمل و کارایی ایمپلنتها، که شامل سلولهای اندودرم پانکراس مشتقشده از سلولهای بنیادی پرتوان انسانی (PSCs) بود، روی 26 بیمار مورد آزمایش قرار گرفت. در حالی که انسولین ترشح شده توسط ایمپلنت ها اثرات بالینی در بیماران نداشت، داده ها اولین شواهد گزارش شده از ترشح انسولین تنظیم شده توسط وعده غذایی توسط سلول های بنیادی تمایز یافته در بیماران انسانی است. نتایج در 2 دسامبر در مجلات ظاهر می شود سلول بنیادی سلولی و سلول گزارش پزشکی.
Eelco de Koning از مرکز پزشکی دانشگاه لیدن، یکی از نویسندگان یک تفسیر همراه منتشر شده در می گوید: “یک نقطه عطف ایجاد شده است. امکان عرضه نامحدود سلول های تولید کننده انسولین به افراد مبتلا به دیابت نوع 1 امید می دهد.” سلول بنیادی سلولی. علیرغم عدم وجود اثرات بالینی مرتبط، این مطالعه نقطه عطف مهمی برای حوزه درمانهای جایگزین سلولی مشتق از PSC انسانی باقی خواهد ماند، زیرا یکی از اولین مواردی است که بقای سلولی و عملکرد آن را یک سال پس از پیوند گزارش میکند.
تقریباً 100 سال پس از کشف هورمون انسولین، دیابت نوع 1 به عنوان یک تشخیص تغییر دهنده زندگی و گاهی اوقات تهدید کننده زندگی باقی می ماند. این بیماری با تخریب سلول های β تولید کننده انسولین در جزایر لانگرهانس پانکراس مشخص می شود که منجر به سطوح بالای گلوکز قند خون می شود.
درمان با انسولین غلظت گلوکز را کاهش می دهد اما آنها را به طور کامل عادی نمی کند. علاوه بر این، سیستمهای تحویل انسولین مدرن میتوانند برای مدت طولانی استفاده شوند، گاهی اوقات دچار اختلال میشوند و اغلب منجر به عوارض طولانیمدت میشوند. در حالی که درمان جایگزینی جزایر می تواند درمانی ارائه دهد زیرا ترشح انسولین را در بدن بازیابی می کند، این روش به طور گسترده ای مورد استفاده قرار نگرفته است زیرا اندام های اهدا کننده کمیاب هستند. این چالش ها بر نیاز به یک منبع جایگزین فراوان از سلول های تولید کننده انسولین تأکید می کند.
استفاده از PSCهای انسانی پیشرفت قابل توجهی در جهت تبدیل شدن به یک گزینه بالینی قابل دوام برای تولید انبوه سلول های تولید کننده انسولین داشته است. در سال 2006، دانشمندان Novocell (اکنون ViaCyte) پروتکل چند مرحلهای را گزارش کردند که تمایز سلولهای بنیادی جنینی انسان را به سلولهای اندودرم پانکراس نابالغ هدایت میکرد. این پروتکل گام به گام که مسیرهای سیگنالینگ کلیدی را دستکاری می کند بر اساس رشد جنینی پانکراس است. مطالعات بعدی نشان داد که این سلولهای آندودرم پانکراس وقتی در مدلهای حیوانی کاشته میشوند، میتوانند بیشتر بالغ شوند و کاملاً عملکردی شوند. بر اساس این نتایج، آزمایشهای بالینی با استفاده از این سلولهای اندودرم پانکراس آغاز شد.
اکنون دو گروه در مورد یک کارآزمایی بالینی فاز I/II گزارش میدهند که در آن سلولهای اندودرم پانکراس در دستگاههای ماکرو کپسولهسازی غیرمحافظ ایمنی (“باز”) قرار داده شدهاند، که اجازه عروقی شدن مستقیم سلولها را میدهد و در زیر پوست در بیماران مبتلا به نوع 1 کاشته میشود. دیابت. استفاده از سلولهای خارج از قفسه شخص ثالث در این استراتژی جایگزینی جزایر مبتنی بر سلولهای بنیادی به عوامل سرکوبکننده ایمنی نیاز دارد که در برابر رد پیوند محافظت میکنند اما میتوانند عوارض جانبی عمدهای مانند سرطان و عفونت ایجاد کنند. شرکتکنندگان تحت یک رژیم درمانی سرکوبکننده ایمنی قرار گرفتند که معمولاً در روشهای پیوند جزایر اهداکننده استفاده میشود.
که در سلول بنیادی سلولیتیموتی کیفر از دانشگاه بریتیش کلمبیا و همکارانش شواهد قانع کننده ای از سلول های عملکردی ترشح کننده انسولین پس از کاشت ارائه کردند. PEC-01s – سلولهای اندودرم پانکراس کاندید دارویی تولید شده توسط ViaCyte – در عرض 26 هفته پس از کاشت، زنده ماندند و به سلولهای پاسخگو به گلوکز و ترشح انسولین بالغ شدند. طی یک سال پیگیری، بیماران 20 درصد نیاز به انسولین را کاهش دادند و 13 درصد زمان بیشتری را در محدوده گلوکز خون هدف سپری کردند. به طور کلی، ایمپلنت ها به خوبی بدون عوارض جانبی شدید مرتبط با پیوند تحمل شدند.
برای اولین بار، ما شواهدی ارائه میکنیم که نشان میدهد PEC-01 مشتق از سلولهای بنیادی میتوانند به سلولهای β بالغ پاسخدهنده به گلوکز و تولید انسولین بالغ شوند. in vivo کیفر می گوید: در بیماران مبتلا به دیابت نوع 1، این یافته های اولیه از سرمایه گذاری و تحقیقات آتی برای بهینه سازی سلول درمانی برای دیابت حمایت می کند.
با این حال، دو بیمار عوارض جانبی جدی مرتبط با پروتکل سرکوب سیستم ایمنی را تجربه کردند. علاوه بر این، هیچ گروه کنترلی وجود نداشت و مداخلات کور نبودند، نتیجهگیریهای علّی محدودکننده، و پیامدها در میان تعداد کمی از شرکتکنندگان بسیار متغیر بود. علاوه بر این، مطالعات بیشتر برای تعیین دوز سلول های اندودرم پانکراس لازم است تا به مزایای بالینی مرتبط برای بیماران دست یابد.
که در سلول گزارش پزشکیهاوارد فویت از ViaCyte و همکارانش پیوند و بیان انسولین را در 63 درصد از دستگاههای کاشته شده از افراد آزمایشی در دورههای زمانی 3 تا 12 ماه پس از کاشت گزارش کردند. تجمع تدریجی سلول های عملکردی و ترشح کننده انسولین در طی یک دوره تقریباً 9-6 ماهه از زمان کاشت رخ داده است.
اکثر عوارض جانبی گزارش شده مربوط به روش های کاشت یا ریزنمونه جراحی یا عوارض جانبی سرکوب کننده سیستم ایمنی بود. علیرغم سرکوب سیستم ایمنی قوی، چندین محل کاشت جراحی و وجود مواد خارجی، خطر عفونت موضعی بسیار کم بود، که نشان میدهد این رویکرد در افرادی که در معرض خطر پاسخ درمانی ضعیف هستند به خوبی قابل تحمل است. محققان در حال حاضر در حال کار بر روی راه هایی برای ترویج عروق پیوند و بقا هستند.
“مطالعه حاضر برای اولین بار در تعداد کمی از افراد مبتلا به دیابت نوع 1 به طور قطع نشان می دهد که سلول های پیش ساز پانکراس مشتق شده از PSC ظرفیت بقا، پیوند، تمایز و بالغ شدن به جزایر مانند انسان را دارند. فویت میگوید که سلولها در صورت کاشت زیر جلدی.
هر دو گزارش نشان دادند که گرافت ها عروقی شده اند و سلول های دستگاه می توانند تا 59 هفته پس از کاشت زنده بمانند. تجزیه و تحلیل پیوندها نشان داد که انواع سلول های جزایر اصلی، از جمله سلول های β، وجود دارند. علاوه بر این، هیچ توموری به نام تراتوم وجود نداشت. با این حال، نسبت انواع مختلف سلول های غدد درون ریز در مقایسه با جزایر بالغ پانکراس غیر معمول بود و درصد کل سلول های انسولین مثبت در دستگاه نسبتاً پایین بود.
با توجه به ایمنی، بیشتر عوارض جانبی شدید با استفاده از عوامل سرکوبگر سیستم ایمنی همراه بود و بر استفاده مادامالعمر از این داروها بهعنوان مانع اصلی برای اجرای گستردهتر این نوع درمانهای جایگزین سلولی تأکید میکرد. فرانسوا کارلوتی از مرکز پزشکی دانشگاه لیدن میگوید: «یک سناریوی ممکن آینده ایدهآل و آفتابی، در دسترس بودن گسترده درمان جایگزین ایمن و کارآمد مبتنی بر سلولهای بنیادی بدون نیاز به این عوامل سرکوبکننده سیستم ایمنی یا روشهای تهاجمی و پرخطر پیوند است.» ، یکی از نویسندگان تفسیر مرتبط.
به گفته دی کونینگ و کارلوتی، بسیاری از سوالات باید پاسخ داده شوند. به عنوان مثال، محققان باید مرحله تمایزی را که در آن سلولها برای پیوند بهینه هستند و بهترین مکان پیوند را تعیین کنند. همچنین مشخص نیست که آیا می توان اثربخشی و ایمنی سلول ها را در طول زمان حفظ کرد و آیا می توان نیاز به درمان سرکوب کننده سیستم ایمنی را از بین برد.
“راه بالینی برای اجرای گسترده درمان جایگزینی جزایر مشتق شده از سلول های بنیادی برای دیابت نوع 1 احتمالا طولانی و پیچیده خواهد بود. تا آن زمان، پیوند پانکراس و جزایر اهدایی گزینه های درمانی مهمی برای گروه کوچکی از بیماران باقی خواهد ماند.” کونینگ می گوید. اما بالاخره عصر کاربرد بالینی درمان جایگزین جزایر مبتنی بر سلول های بنیادی برای درمان دیابت آغاز شده است.
سلول های بتا از سلول های بنیادی: پتانسیل برای درمان جایگزینی سلولی
تیموتی جی کیفر، سلول های اندودرم پانکراس مشتق از سلول های بنیادی پرتوان کاشته شده، پپتید C پاسخگو به گلوکز را در بیماران مبتلا به دیابت نوع 1 ترشح می کنند. سلول بنیادی سلولی (2021). DOI: 10.1016/j.stem.2021.10.003. www.cell.com/cell-stem-cell/fu … 1934-5909(21)00415-X
هاوارد فویت، بیان انسولین و پپتید C در افراد دیابتی نوع 1 کاشته شده با سلولهای اندودرم پانکراس مشتق از سلولهای بنیادی در دستگاه کپسولهسازی، سلول گزارش پزشکی (2021). DOI: 10.1016/j.xcrm.2021.100466. www.cell.com/cell-reports-medi … 2666-3791(21)00338-4
نقل قول: ایمپلنت های مبتنی بر سلول های بنیادی با موفقیت انسولین را در بیماران مبتلا به دیابت نوع 1 ترشح می کنند (2021، 2 دسامبر) بازیابی شده در 2 دسامبر 2021 از https://medicalxpress.com/news/2021-12-stem-cell-based-implants-successfully- secrete.html
این برگه یا سند یا نوشته تحت پوشش قانون کپی رایت است. به غیر از هرگونه معامله منصفانه به منظور مطالعه یا تحقیق خصوصی، هیچ بخشی بدون اجازه کتبی قابل تکثیر نیست. محتوای مذکور فقط به هدف اطلاع رسانی ایجاد شده است.